服务热线
搜题▪组卷
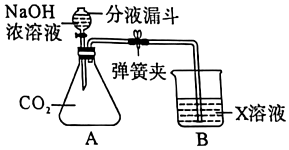
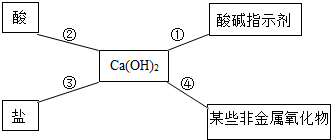
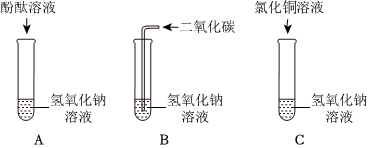
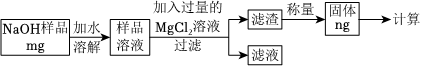
| 实验 | 实验1 | 实验2 | 实验3 | 实验4 |
| 实验操作 | 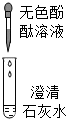 |
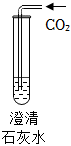 |
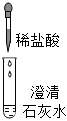 |
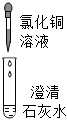 |
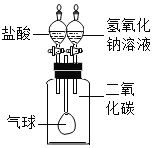
| 现象 | 溶液变红色 | 石灰水变浑浊 | 无明显现象 | 生成蓝色沉淀 |
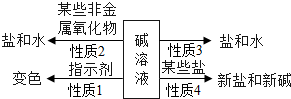
| 结论或解释 | 氢氧化钙能与酚酞等酸碱指示剂反应 | CO2能与氢氧化钙反应 | / | 氢氧化钙能与某些盐反应 |
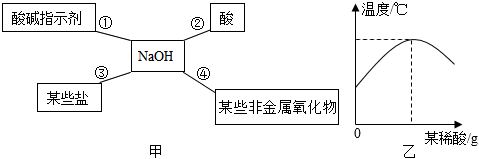

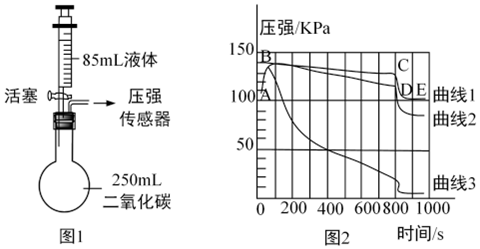
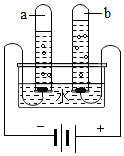 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。
在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。
fv@dyw.com
2023-04-09
初中化学 | | 填空题