[考点]
合金与合金的性质,金属与氧气的反应,金属与酸的反应原理,金属活动性强弱的判断,
[答案]
(1)大;
(2)氧气、水;
(3)Fe+2HCl=FeCl2+H2↑;
(4)AD。
[解析]
解:(1)合金的硬度比组成合金的纯金属的硬度大,越王勾践剑剑身材料(剑身主要含有铜、锡,另外含有少量铁、铝)与纯铜相比,具有硬度大的优良性能。
(2)越王勾践剑在出土时剑身未被腐蚀的原因之一是剑身与剑鞘之间的吻合度极高,有效隔绝了剑身与氧气、水的直接接触。
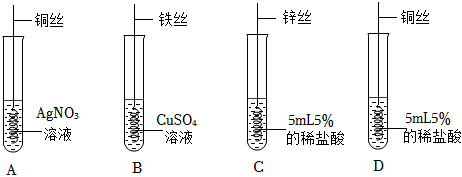
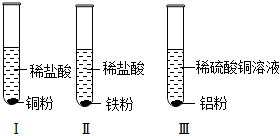
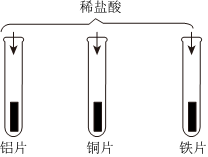
(3)将打磨过的铜片、铁片、铝片分别插入稀盐酸中,铜和稀盐酸不反应,铁和盐酸反应生成氯化亚铁和氢气,铝和盐酸反应生成氯化铝和氢气,反应的化学方程式分别为:Fe+2HCl=FeCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑。
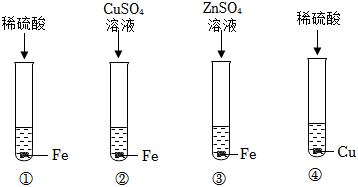
(4)A、铜片和稀硫酸、硫酸亚铁溶液都不反应,无法验证铜、铁、铝的金属活动性顺序,故选项符合题意;
B、铜片和硫酸亚铁溶液不反应,说明金属活动性铁>铜,铝片和硫酸亚铁溶液反应生成硫酸铝和铁,说明金属活动性铝>铁,能验证铜、铁、铝的金属活动性顺序为:铝>铁>铜,故选项不符合题意;
C、铁片和硫酸铜溶液反应生成硫酸亚铁和铜,说明金属活动性铁>铜,铁片和硫酸铝溶液不反应,说明金属活动性铝>铁,能验证铜、铁、铝的金属活动性顺序为:铝>铁>铜,故选项不符合题意;
D、铜片、铁片都不能和硫酸铝溶液反应,无法验证铜、铁、铝的金属活动性顺序,故选项符合题意;
故选项:AD。
故答案为:
(1)大;
(2)氧气、水;
(3)Fe+2HCl=FeCl2+H2↑;
(4)AD。
[点评]
本题考查了"合金与合金的性质,金属与氧气的反应,金属与酸的反应原理,金属活动性强弱的判断,",属于"综合题",熟悉题型是解题的关键。
 “神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。
“神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。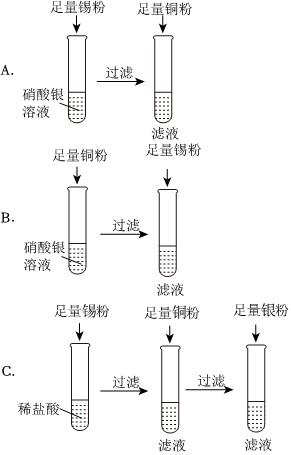
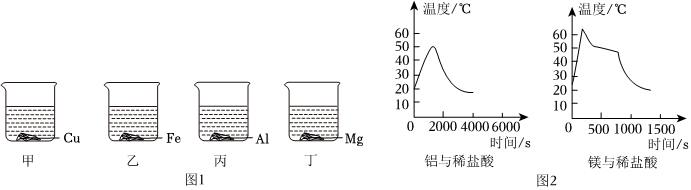
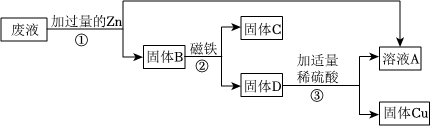
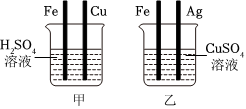
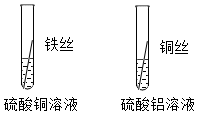 铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验:
铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验: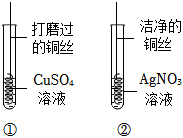 根据金属的性质回答下列问题。
根据金属的性质回答下列问题。 实验中一个能发生反应的化学方程式 。
实验中一个能发生反应的化学方程式 。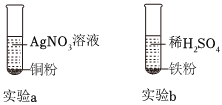 三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题:
三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题: