[考点]
氯化钠与粗盐提纯,盐的化学性质,物质的元素组成,海水的淡化问题,
[答案]
(1)元素;
(2)过滤;
(3)5;
(4)HCl+NaOH=NaCl+H2O或Na2CO3+2HCl=2NaCl+H2O+CO2↑。
[解析]
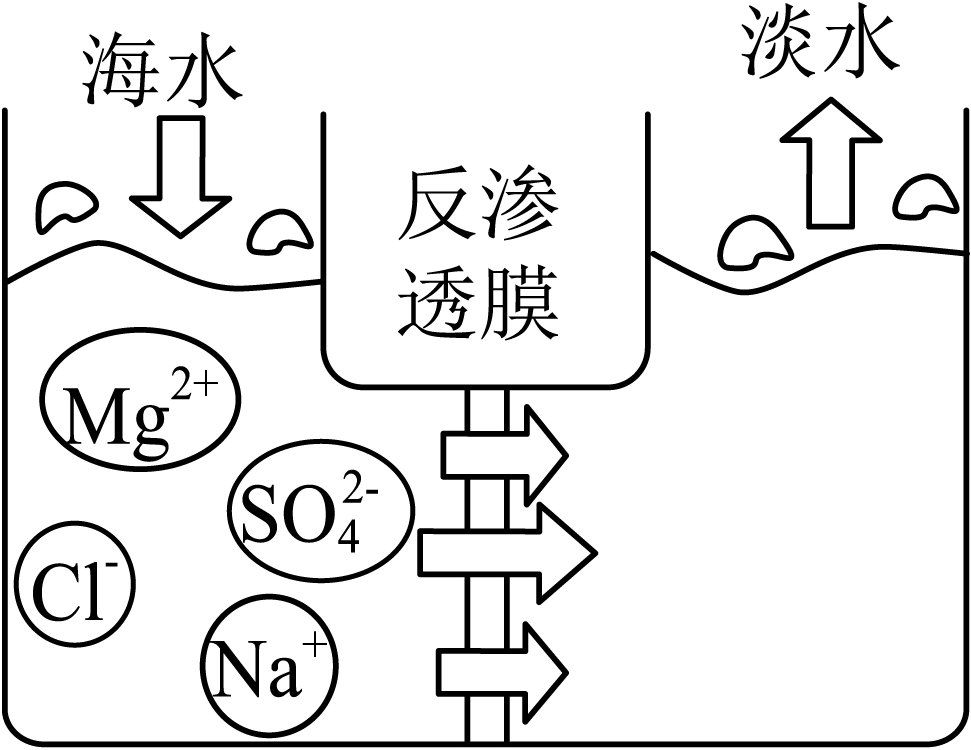
解:(1)海水中的氯、钠、镁、钾、溴等是以化合物的形式存在于海水中,描述的是宏观概念,所以这里应填“元素”;
(2)过滤是将不溶性固体和液体分离,这里膜分离法是通过膜将海水中的离子等溶质与水分离,类似于实验室中的过滤操作;
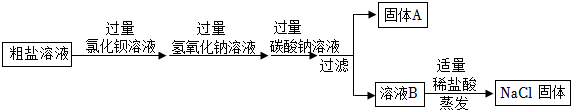
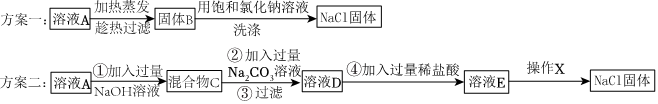
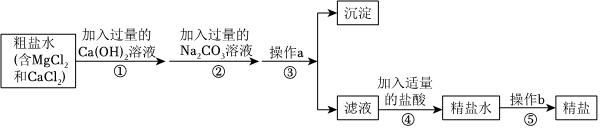
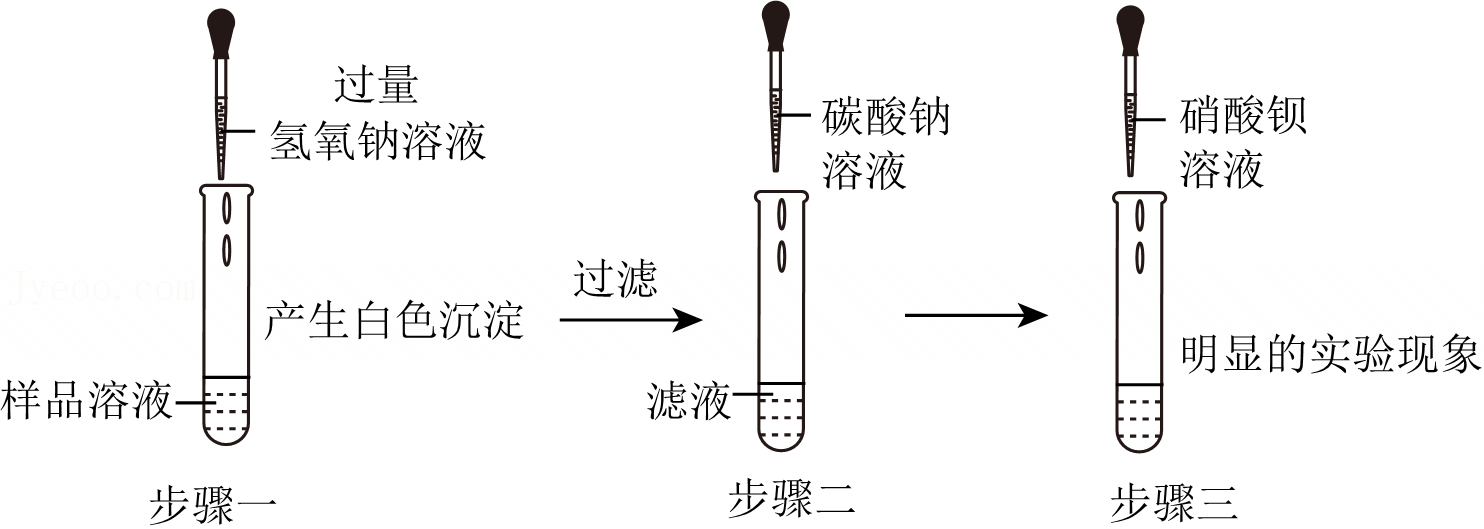
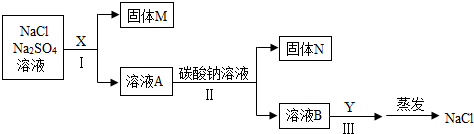
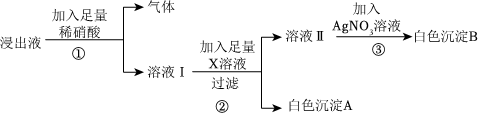
(3)氯化钡能与硫酸钠反应生成氯化钠和硫酸钡白色沉淀;氢氧化钠与氯化镁反应生成氢氧化镁白色沉淀和氯化钠;碳酸钠能与氯化钙反应生成碳酸钙白色沉淀和氯化钠,还能与过量的氯化钡反应生成碳酸钡白色沉淀和氯化钠,泥沙本身不溶于水,经过过滤后,固体A中含有BaSO4、Mg(OH)2、CaCO3、BaCO3和泥沙;共5种物质;
(4)溶液B中存在氢氧化钠、碳酸钠和氯化钠,盐酸与氢氧化钠反应生成氯化钠和水,与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式分别为:HCl+NaOH=NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑。
故答案为:(1)元素;
(2)过滤;
(3)5;
(4)HCl+NaOH=NaCl+H2O或Na2CO3+2HCl=2NaCl+H2O+CO2↑。
[点评]
本题考查了"氯化钠与粗盐提纯,盐的化学性质,物质的元素组成,海水的淡化问题,",属于"综合题",熟悉题型是解题的关键。
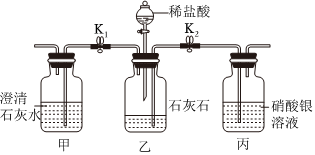
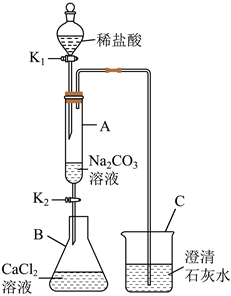 用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。
用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。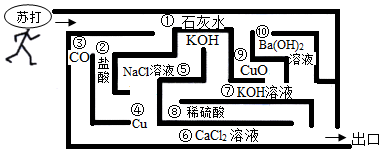

 ?
?
