[考点]
金属的化学性质,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)Zn>X>Cu>Ag;
(2)三;银;
(3)Cu+2AgNO3=Cu(NO3)2+2Ag。
[解析]
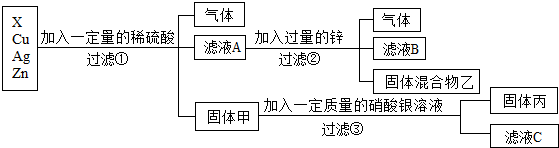
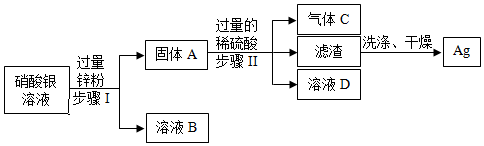
解:(1)向金属混合物中加入一定量的稀硫酸,得到气体、滤液A和固体甲,锌能与稀硫酸反应生成硫酸锌和氢气,铜、银和稀硫酸不反应,向滤液A中加入过量的锌,得到固体混合物乙,说明X能与稀硫酸反应,锌能与X的硫酸盐反应,说明锌比X活泼,X能与稀硫酸反应,则在金属活动性顺序里,X排在氢前,铜、银排在氢后,故四种金属的活动性由强到弱的顺序是:Zn>X>Cu>Ag;
(2)由以上分析可知,向金属混合物中加入一定量稀硫酸,锌能与稀硫酸反应生成硫酸锌和氢气,X能与稀硫酸反应生成X的硫酸盐和氢气,向滤液A中加入过量的锌,得到气体,说明滤液A中含硫酸,故滤液A中含硫酸锌、硫酸、X的硫酸盐三种溶质。固体甲为铜和银的混合物,向固体甲中加入一定质量的硝酸银,铜和硝酸银反应生成硝酸铜和银,故固体丙中一定含银,无法确定是否含有铜。
(3)③发生的反应是硝酸银和铜反应生成硝酸铜和银,化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag。
故答案为:(1)Zn>X>Cu>Ag;
(2)三;银;
(3)Cu+2AgNO3=Cu(NO3)2+2Ag。
[点评]
本题考查了"金属的化学性质,书写化学方程式、文字表达式、电离方程式,",属于"必考题",熟悉题型是解题的关键。
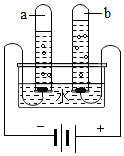 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。
在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。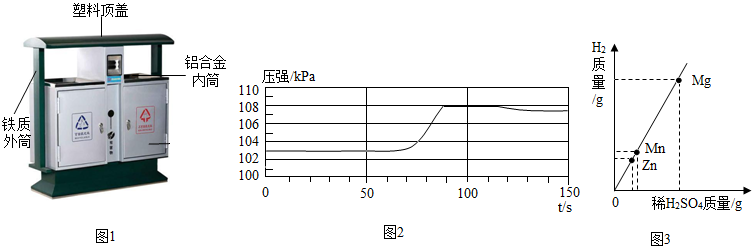 (1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。
(1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。