[考点]
过滤所需的仪器,盐的化学性质,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)2NaOH+MgSO4=Mg(OH)2↓+Na2SO4;
(2)H2SO4;
(3)C。
[解析]
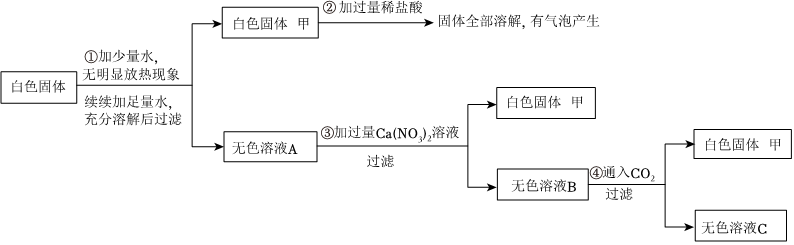
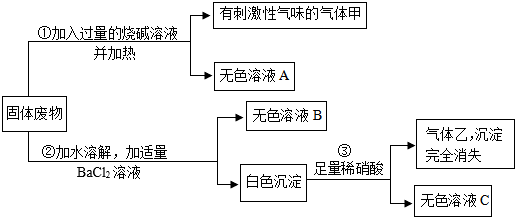
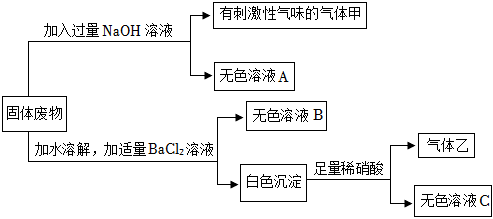
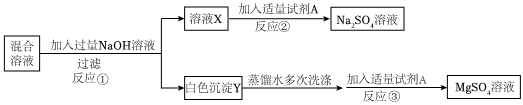
解:Na2SO4和MgSO4的混合溶液中加入过量氢氧化钠溶液,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,则白色沉淀Y是氢氧化镁,溶液X中含有硫酸钠和氢氧化钠,加入试剂A得到硫酸钠溶液,则A为稀硫酸,硫酸和氢氧化钠反应生成硫酸钠和水。
(1)反应①:硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,化学方程式为:2NaOH+MgSO4=Mg(OH)2↓+Na2SO4;
(2)综上分析,试剂A是稀硫酸,化学式为H2SO4;
(3)A、过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗,故A错误;
B、硫酸镁和氢氧化钠反应生成氢氧化镁沉淀,氢氧化镁和硫酸反应生成硫酸镁,根据质量守恒定律,若不考虑操作过程中的损失,最终溶液中 MgSO4和初始溶液中 MgSO4相等,故B错误;
C、蒸发可以将溶质从溶液中分离出来,故C正确。
故选:C。
故答案为:(1)2NaOH+MgSO4=Mg(OH)2↓+Na2SO4;
(2)H2SO4;
(3)C。
[点评]
本题考查了"过滤所需的仪器,盐的化学性质,书写化学方程式、文字表达式、电离方程式,",属于"典型题",熟悉题型是解题的关键。
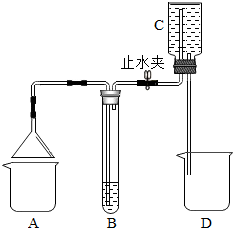
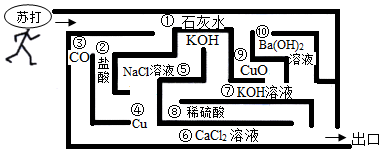
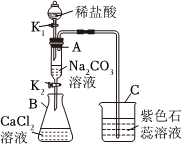
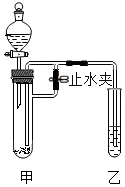 某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.
某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.