[解析]
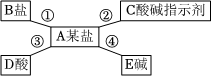
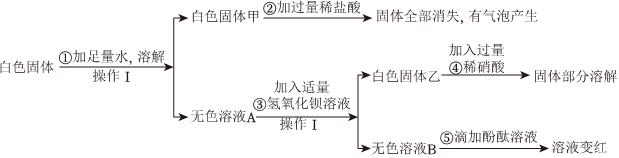
解:(1)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl;
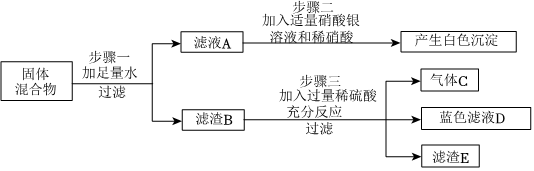
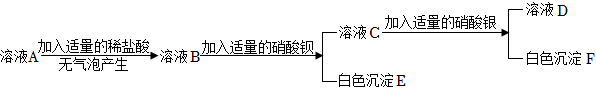
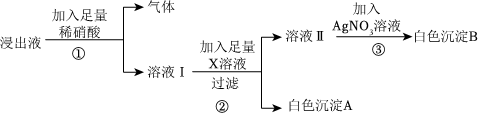
(2)A、碳酸钠和硝酸钡反应生成溶于酸的碳酸钡沉淀,硫酸钠和硝酸钡反应生成不溶于酸的硫酸钡沉淀,取样品,滴加过量的硝酸钡溶液,产生白色沉淀,继续加入过量的稀硝酸,观察到沉淀部分消失,产生气泡,消失的是碳酸钡沉淀,不能溶于酸的是硫酸钡沉淀,说明碳酸钠溶液中一定混有硫酸钠,故A正确;
B、取样于试管中,滴加硝酸银溶液,产生白色沉淀,可能是氯化钠和硝酸银反应生成氯化银沉淀,可能是碳酸钠和硝酸银反应生成的同时银沉淀,不能说明碳酸钠溶液中一定混有氯化钠,故B错误;
C、氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,对样品中的氯化钠的检验造成干扰,故C错误。
故选:A。
故答案为:(1)BaCl2+Na2CO3=BaCO3↓+2NaCl;
(2)A。
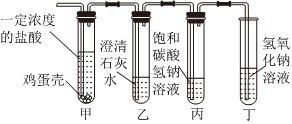
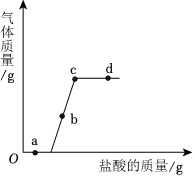
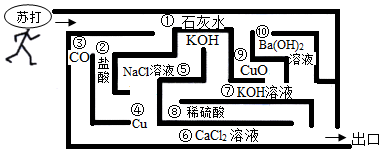
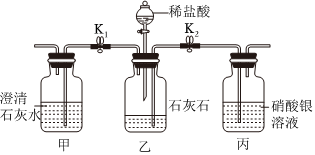
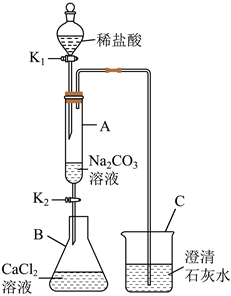 用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。
用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。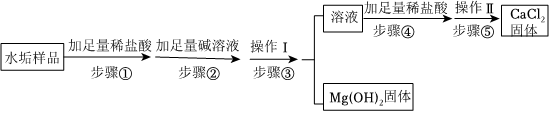
 ?
?