[考点]
饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度的概念,
[答案]
(1)NaCl;
(2)53.9;
(3)不饱和;60。
[解析]
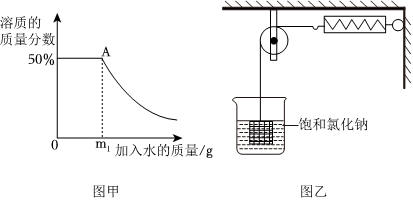
解:(1)20℃时,氯化钠的溶解度大于硝酸钾,则氯化钠的饱和溶液的溶质质量分数大于硝酸钾,所以等质量的硝酸钾和氯化钠饱和溶液中,所含溶质质量较多的是NaCl。
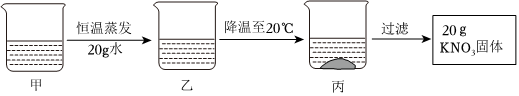
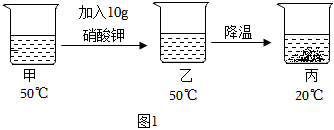
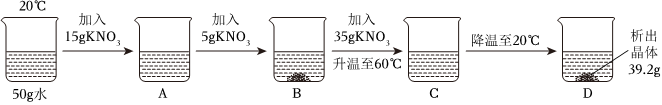
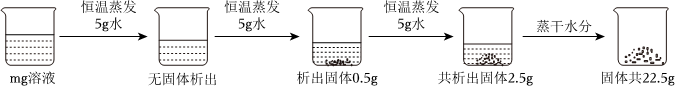
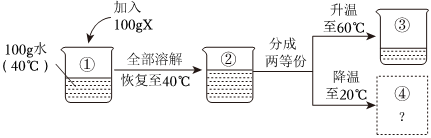
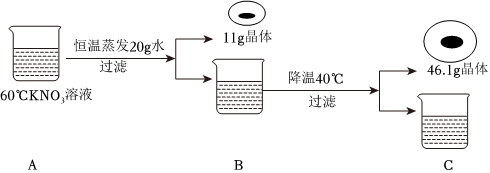
(2)50℃时,硝酸钾的溶解度是85.5g,将175.5g的硝酸钾溶液加入10g硝酸钾后恰好饱和,此时溶液中有100g水,85.5g硝酸钾,降温到20℃,硝酸钾的溶解度变成31.6g,则丙中析出的硝酸钾固体质量为:85.5g﹣31.6g=53.9g。
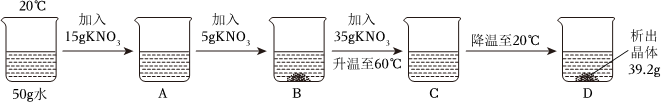
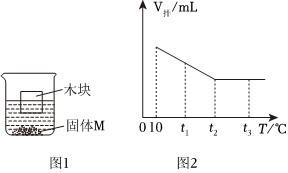
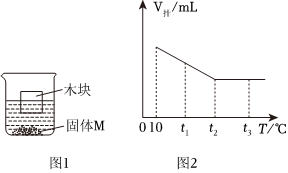
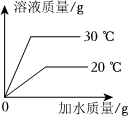
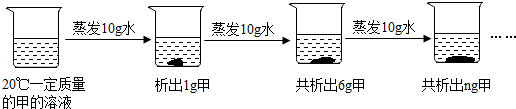
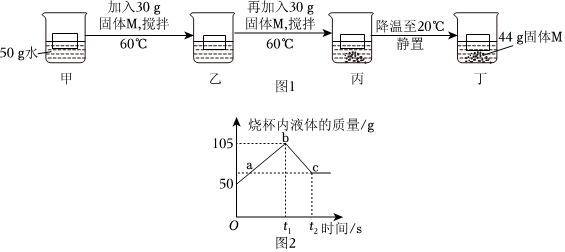
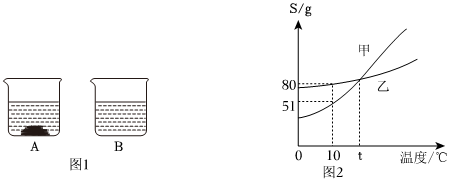
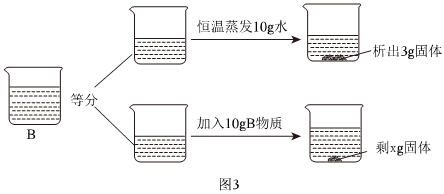
(3)t℃时,将一定质量的硝酸钾溶液恒温蒸发溶剂,蒸发溶剂质量与析出晶体质量的关系如图2所示。①蒸发10g水,没有晶体析出,再蒸发10g水,析出5.5g晶体,再蒸发10g水,析出16.5g﹣5.5g=11g晶体,说明该温度下,10g中最多能溶解11g硝酸钾,从A到B蒸发了10g水只析出5.5g晶体,说明A点对应的溶液是不饱和溶液;②10g中最多能溶解11g硝酸钾,则100g中最多能溶解110g硝酸钾,所以该温度下硝酸钾的溶解度为110g,由表中数据可知,t℃=60℃。
故答案为:
(1)NaCl;
(2)53.9;
(3)不饱和;60。
[点评]
本题考查了"饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度的概念,",属于"典型题",熟悉题型是解题的关键。

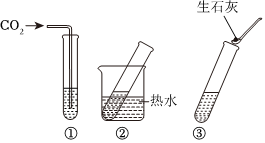
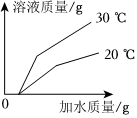
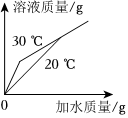
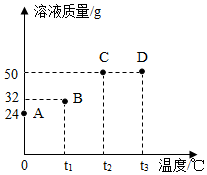 将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得溶液的质量分别如图中A、B、C、D点所示。回答下列问题:(1)0℃时,物质X的溶解度是 。
将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得溶液的质量分别如图中A、B、C、D点所示。回答下列问题:(1)0℃时,物质X的溶解度是 。
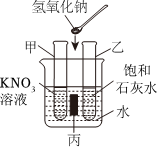
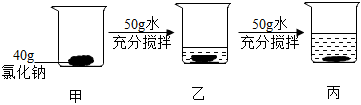
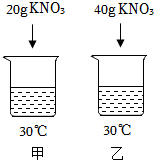 已知10℃时KNO3的溶解度为20.9g,30℃时KNO3的溶解度为45.8g。如图,小明同学在盛有100g30℃蒸馏水的甲、乙两个烧杯中分别加入20g和40gKNO3固体,充分溶解。请回答下列问题:
已知10℃时KNO3的溶解度为20.9g,30℃时KNO3的溶解度为45.8g。如图,小明同学在盛有100g30℃蒸馏水的甲、乙两个烧杯中分别加入20g和40gKNO3固体,充分溶解。请回答下列问题: