[考点]
二氧化碳的实验室制法,二氧化碳的化学性质,
[答案]
(1)CaCO3+2HCl═CaCl2+CO2↑+H2O;
(2)1号滤纸条不变,2号滤纸条变红;
(3)二氧化碳既不能燃烧,也不能支持燃烧;
(4)C;
(5)饱和NaHCO3。
[解析]
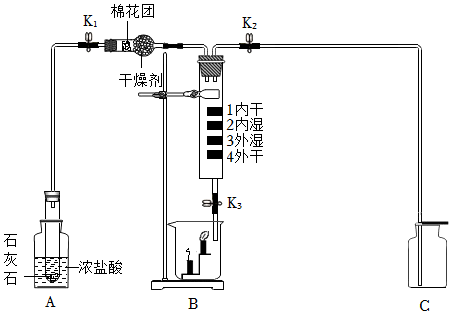
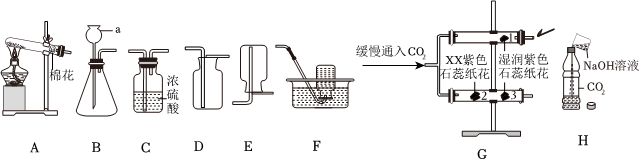
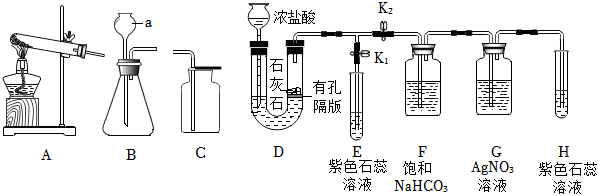
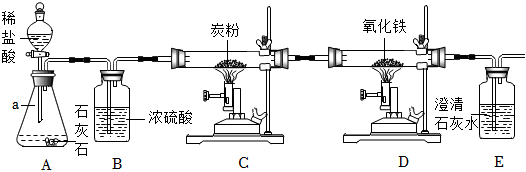
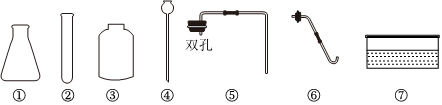
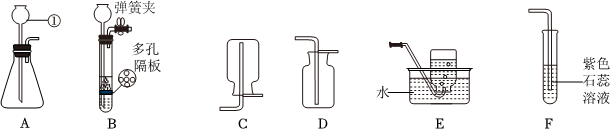
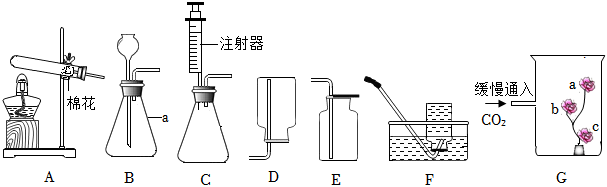
解:(1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O;
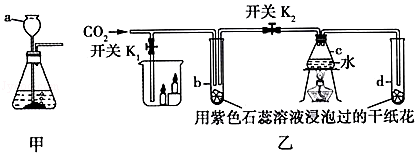
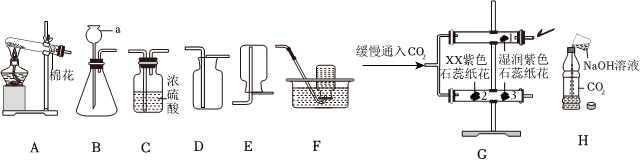
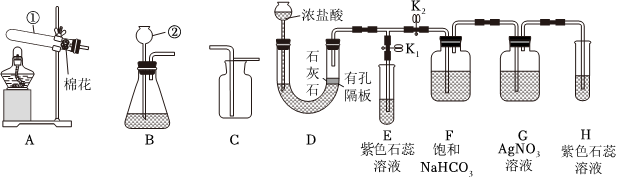
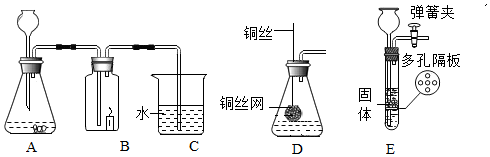
(2)装置B玻璃管内、外壁分别贴有用紫色石蕊试液浸泡过的滤纸条,打开k1,关闭k2和k3,并向玻璃管外壁上4号滤纸条喷醋酸,观察到:1号滤纸条不变,2号滤纸条变红,3号滤纸条不变,4号滤纸条变红,由此证明了CO2能与水反应;故答案为:1号滤纸条不变,2号滤纸条变红;
(3)紧接着又打开k3观察到低处蜡烛先熄灭,则说明CO2具有的化学性质是:二氧化碳既不能燃烧,也不能支持燃烧;故答案为:二氧化碳既不能燃烧,也不能支持燃烧;
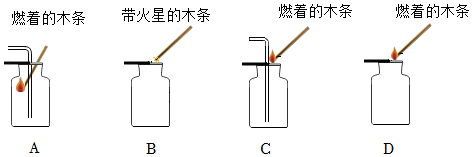
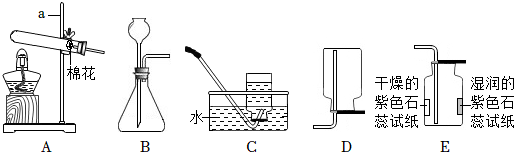
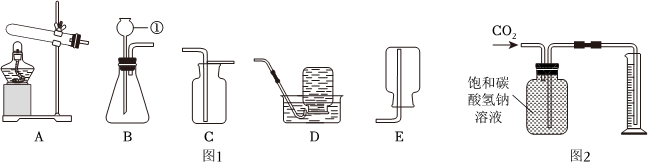
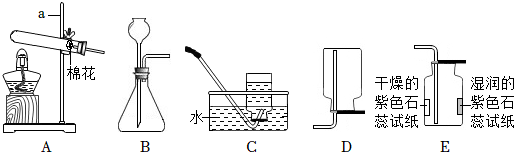
(4)如图所示CO2验满操作中,正确的是C,因为应该燃着的木条放在瓶口,验满之前短管不能拿出;故答案为:C;
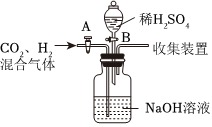
(5)为保证制得纯净的二氧化碳,棉花团上应事先浸有饱和NaHCO3溶液,因为饱和NaHCO3溶液吸收氯化氢气体;故答案为:饱和NaHCO3。
[点评]
本题考查了"二氧化碳的实验室制法,二氧化碳的化学性质,",属于"易错题",熟悉题型是解题的关键。