[考点]
金属的物理性质及用途,金属的化学性质,金属活动性顺序及其应用,金属锈蚀的条件及其防护,
[答案]
(1)4Al+3O2=2Al2O3;
(2)延展性;
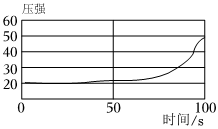
(3)隔绝水和氧气;
(4)D;
(5)BD。
[解析]
解:(1)铝耐腐蚀的原因是,铝和空气中的氧气反应产生一层致密的氧化铝薄膜,阻止铝的进一步氧化,反应的化学方程式为:4Al+3O2=2Al2O3;
(2)金制成较薄的面具,体现了金良好的延展性;
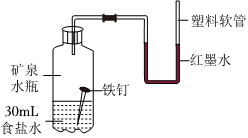
(3)跨海大桥在施工的过程中,通常采用高性能环氧涂层防止生锈,其防锈原理是隔绝水和氧气;
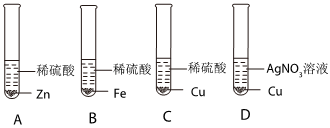
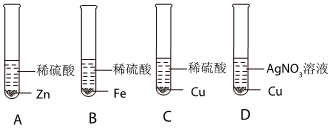
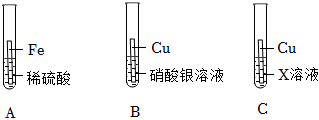
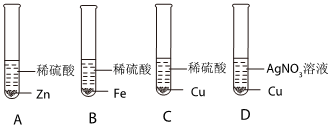
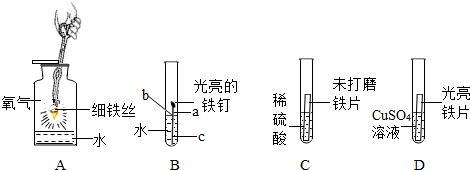
(4)在验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属的盐溶液与两端金属的单质反应或取中间金属单质与两端的金属的盐溶液反应;
A.铁能和硫酸铜反应生成铜,银不会和硫酸铜溶液反应,金属活动性顺序为铁大于铜大于银,可行;
B.铁和盐酸、硝酸银溶液反应,铜和稀盐酸不反应、和硝酸银生成银单质,说明活动性顺序铁大于氢大于铜大于银,可行;
C.铜和氯化亚铁溶液不反应、和硝酸银溶液生成银单质,金属活动性顺序为铁大于铜大于银,可行;
D.铜、银与稀盐酸均不反应,不能判断两者的活动性,不可行;
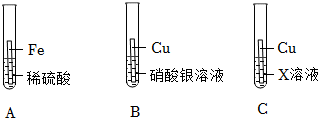
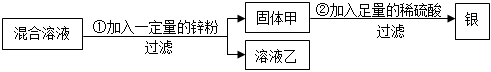
(5)青铜是铜的合金,合金比组成它的纯金属硬度大,向一定质量的Fe(NO3)2和AgNO3的混合溶液中加入一定量锌粉,锌首先和硝酸银生成银和硝酸锌、再和硝酸亚铁生成铁和硝酸锌;
A、若滤液为浅绿色,说明存在硝酸亚铁,则滤渣中不可能有锌,错误;
B、滤液中一定有生成的Zn(NO3)2,滤渣中一定有生成的银,正确;
C、若取少量滤液,加入稀盐酸,无明显现象,说明滤液中没有硝酸银,则滤渣中一定有银,无法确定是否含有铁,错误;
D、铁、锌均和稀盐酸生成氢气;若取少量滤渣,加入稀盐酸,产生气泡,则滤渣中一定含有银、铁,可能含有过量锌,故组成有银、铁或银、铁、锌2种情况,正确;
故答案为:(1)4Al+3O2=2Al2O3;
(2)延展性;
(3)隔绝水和氧气;
(4)D;
(5)BD。
[点评]
本题考查了"金属的物理性质及用途,金属的化学性质,金属活动性顺序及其应用,金属锈蚀的条件及其防护,",属于"综合题",熟悉题型是解题的关键。
 ?
? ?
?

 ?
? ?
?
 ?
?