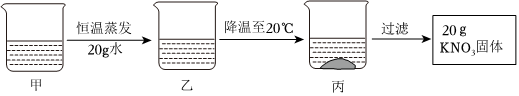
[考点]
饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度的影响因素,溶解度的相关计算,配制一定溶质质量分数的计算,
[答案]
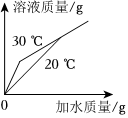
(1)蔗糖的溶解度随着温度的升高而增大;
(2)①饱和;②1.5;③>;
(3)119。
[解析]
解:(1)根据蔗糖和小苏打的溶解度表可知,蔗糖的溶解度随着温度的升高而增大。
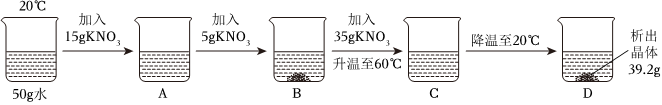
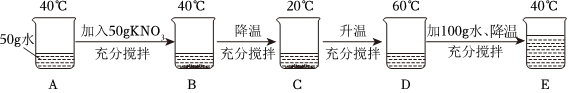
(2)①20℃时,小苏打的溶解度为9.6g,即20℃时,100g水中最多能溶解9.6g小苏打,达到饱和状态。a温度为20℃,溶剂水的质量为100g,加入小苏打5g<9.6g,则a为该温度下的不饱和溶液,b再加入4.6g小苏打,加入小苏打的总质量为5g+4.6g=9.6g,则b中溶液恰好是小苏打的饱和溶液。
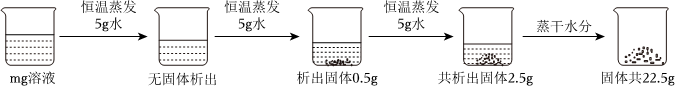
②c中继续加入50g蔗糖,降温至10℃,溶剂水的质量不变还是100g,小苏打和蔗糖的溶解度均减小,d中有固体析出,10℃时,小苏打的溶解度为8.1g,<9.6g,蔗糖的溶解度为191g,>50g,则析出小苏打的质量为9.6g﹣8.1g=1.5g,蔗糖不会析出,所以析出固体的质量为1.5g。
③由①解析可知,b中溶剂水的质量为100g,溶质小苏打的质量为9.6g,为该温度下恰好饱和溶液,c中溶剂水的质量为100g,溶质小苏打的质量为9.6g,20℃时蔗糖的溶解度为204g,>50g,则c中加入50g蔗糖能完全溶解,b、c中溶质小苏打的质量不变,溶液质量b<c,则瓶内溶液中小苏打的质量分数:b>c。
(3)40℃时,蔗糖的溶解度为238g,欲配制169g蔗糖饱和溶液,需要取用蔗糖的质量为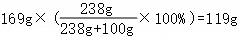 。
故答案为:
(1)蔗糖的溶解度随着温度的升高而增大;
(2)①饱和;②1.5;③>;
(3)119。
。
故答案为:
(1)蔗糖的溶解度随着温度的升高而增大;
(2)①饱和;②1.5;③>;
(3)119。
[点评]
本题考查了"饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度的影响因素,溶解度的相关计算,配制一定溶质质量分数的计算,",属于"压轴题",熟悉题型是解题的关键。
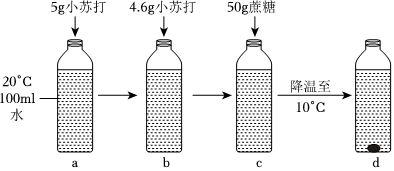
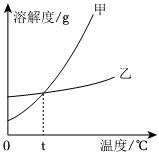 列表法和作图法是常用的数据处理方法。请根据下列图表进行分析。
列表法和作图法是常用的数据处理方法。请根据下列图表进行分析。