服务热线
搜题▪组卷
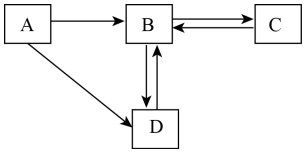
 现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为某重地的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分。(提示:碳酸钡不溶于水)
现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为某重地的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分。(提示:碳酸钡不溶于水)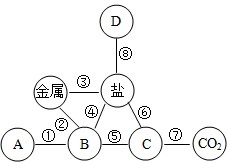
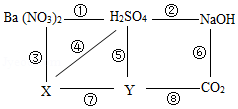
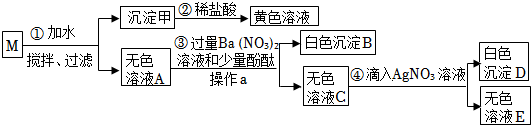
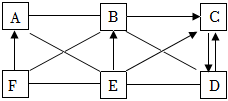 图中A~F为6种初中化学常见的物质,其中B是胃液的主要成分,C为一种常见溶剂,D可用于改良酸性土壤,F是一种红棕色的氧化物。各物质间的反应及转化关系如图所示(“—”表示两种物质间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应物、生成物、反应条件已略去)请回答:
图中A~F为6种初中化学常见的物质,其中B是胃液的主要成分,C为一种常见溶剂,D可用于改良酸性土壤,F是一种红棕色的氧化物。各物质间的反应及转化关系如图所示(“—”表示两种物质间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应物、生成物、反应条件已略去)请回答: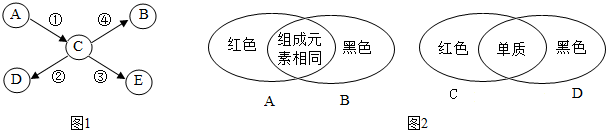

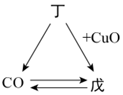
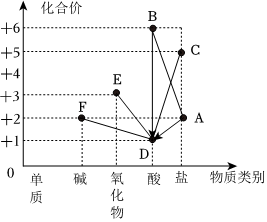 常见物质A→F中某种元素的化合价与物质类别的关系如图(“→”表示物质之间可以转化,“—”表示相连的物质能发生反应,部分反应物、生成物已省略)。其中D与E反应可清除铁制品表面的铁锈,F为蓝色固体。
常见物质A→F中某种元素的化合价与物质类别的关系如图(“→”表示物质之间可以转化,“—”表示相连的物质能发生反应,部分反应物、生成物已省略)。其中D与E反应可清除铁制品表面的铁锈,F为蓝色固体。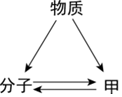 |
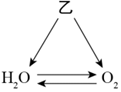 |
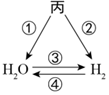 |
 |
| (1)题图 | (2)题图 | (3)题图 | (4)题图 |
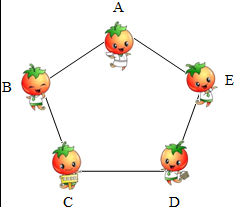
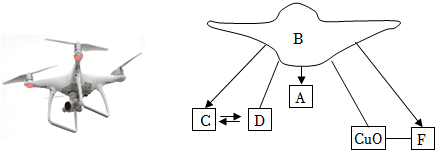
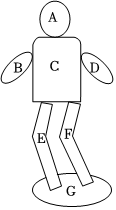 2025年春晚机器人节目的出现不仅是科技与艺术融合的生动体现,也为文化传播、教育发展和未来社会的科技应用提供了重要启示。如图是化学兴趣小组同学利用化学物质构建的机器人模型,其中A~G分别是稀盐酸、氢氧化钙、碳酸钙、氢氧化钠、铁、氧化铜、氯化镁七种物质中的一种。A为大理石的主要成分,B含有两种元素,人体胃液中含有C,相邻的物质之间能发生化学反应(所涉及反应均为初中常见的化学反应),请回答下列问题:
2025年春晚机器人节目的出现不仅是科技与艺术融合的生动体现,也为文化传播、教育发展和未来社会的科技应用提供了重要启示。如图是化学兴趣小组同学利用化学物质构建的机器人模型,其中A~G分别是稀盐酸、氢氧化钙、碳酸钙、氢氧化钠、铁、氧化铜、氯化镁七种物质中的一种。A为大理石的主要成分,B含有两种元素,人体胃液中含有C,相邻的物质之间能发生化学反应(所涉及反应均为初中常见的化学反应),请回答下列问题: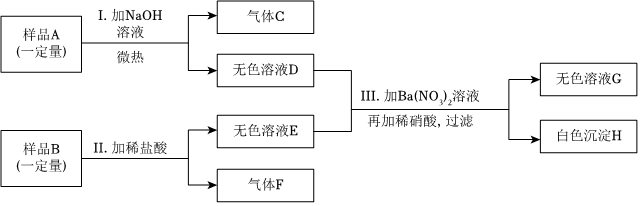

jsx@dyw.com
2017-03-22
初中化学 | | 填空题