服务热线
搜题▪组卷
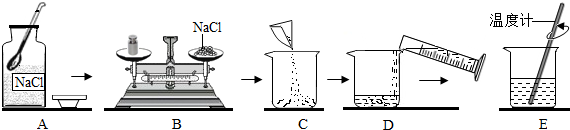
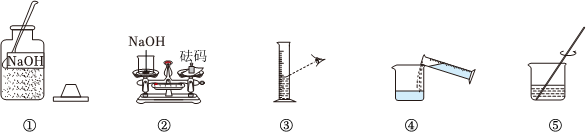 ?
?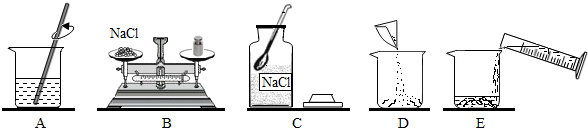
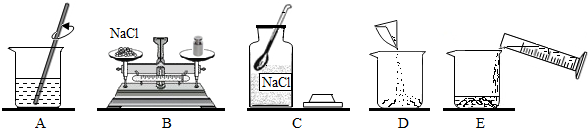
 ?
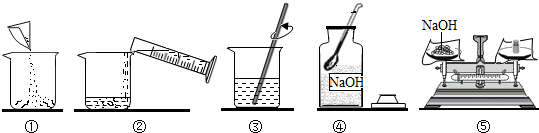
?| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量/g | 45 | 50 | 55 | 60 |
| 所得溶液的质量/g | 95 | 100 | 105 | 105 |
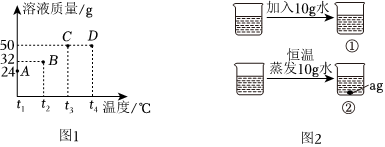

| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
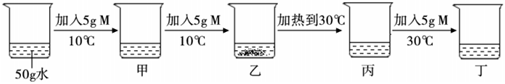
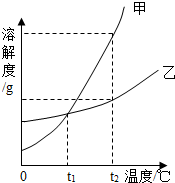 如图是甲、乙两种物质的溶解度曲线,回答下列问题:
如图是甲、乙两种物质的溶解度曲线,回答下列问题: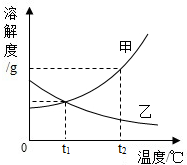 图是甲、乙两种固体物质的溶解度曲线.
图是甲、乙两种固体物质的溶解度曲线.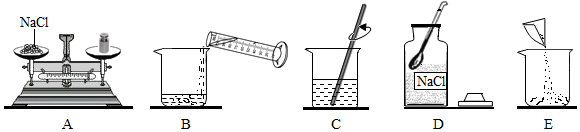
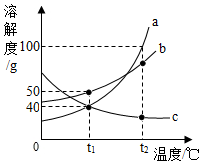 如图所示,a、b、c为三种物质的溶解度曲线,请根据图示信息回答下列问题。
如图所示,a、b、c为三种物质的溶解度曲线,请根据图示信息回答下列问题。| 温度/℃ | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
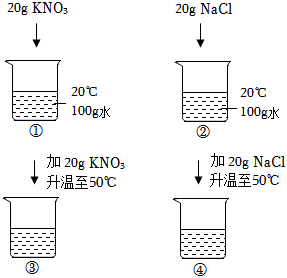
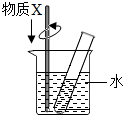
| 选项 | A | B | C |
| 试管内溶液中的溶质 | KNO3 | Ca(OH)2 | KNO3 |
| 物质X | NaCl | 浓硫酸 | NH4NO3 |
 体验蛋雕艺术,传承非遗文化。兴趣小组用化学方法制作蛋雕:将蛋壳在熔化的石蜡中裹上蜡衣,用金属丝划穿蜡衣雕刻出花纹,吸取稀盐酸滴在划痕处,一段时间后放入热水中熔去多余的蜡,做成蛋雕作品。
体验蛋雕艺术,传承非遗文化。兴趣小组用化学方法制作蛋雕:将蛋壳在熔化的石蜡中裹上蜡衣,用金属丝划穿蜡衣雕刻出花纹,吸取稀盐酸滴在划痕处,一段时间后放入热水中熔去多余的蜡,做成蛋雕作品。
zc@dyw.com
2019-04-07
初中化学 | | 填空题