服务热线
搜题▪组卷
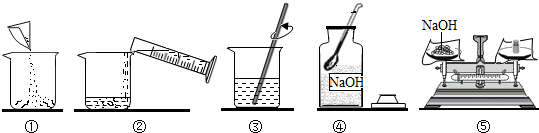
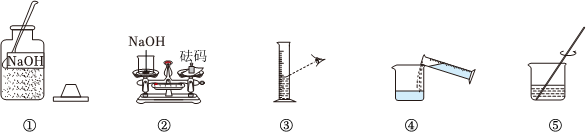 ?
?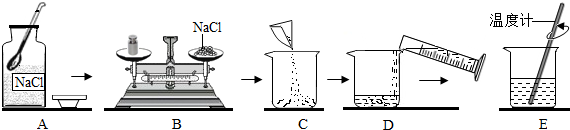
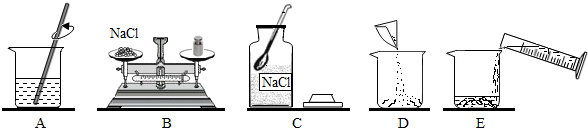
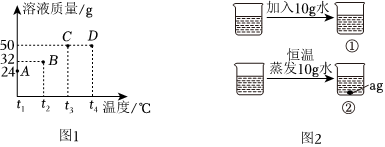

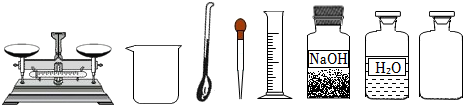 ?
?| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量/g | 45 | 50 | 55 | 60 |
| 所得溶液的质量/g | 95 | 100 | 105 | 105 |
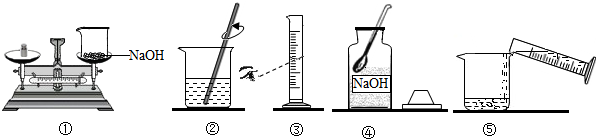
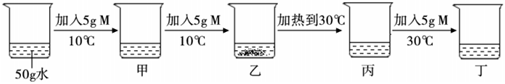
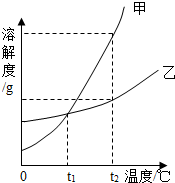 如图是甲、乙两种物质的溶解度曲线,回答下列问题:
如图是甲、乙两种物质的溶解度曲线,回答下列问题:| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
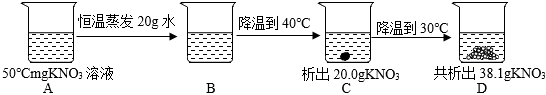
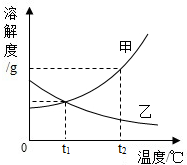 图是甲、乙两种固体物质的溶解度曲线.
图是甲、乙两种固体物质的溶解度曲线.
bjj@dyw.com
2013-04-15
初中化学 | | 填空题