[考点]
金属的化学性质,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式,
[答案]
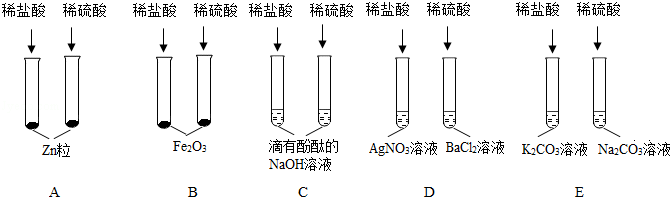
(1)Fe+2HCl=FeCl2+H2↑;
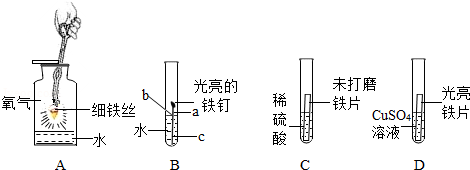
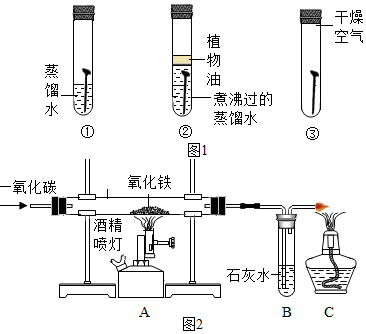
(2)隔绝氧气和水;
(3)2;
(4)能耗较低(合理即可)。
[解析]
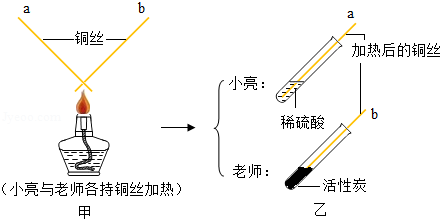
解:(1)铁锈的主要成分有氧化铁,其与盐酸反应氯化铁和水,当铁锈完全反应后,铁接触到了稀盐酸,发生反应生成氯化亚铁和氢气,方程式为:Fe+2HCl=FeCl2+H2↑;
(2)将涂料均匀地涂抹在铁制品外表并使之形成一层连续、致密的涂膜,能够隔绝氧气和水,来防止钢铁锈蚀;
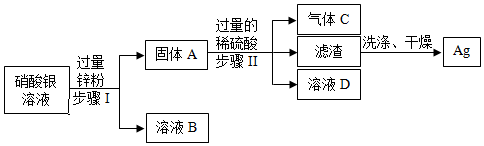
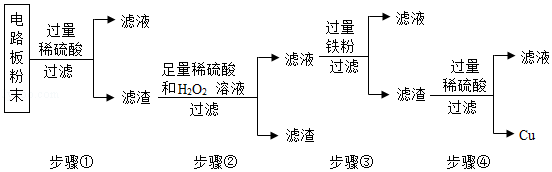
(3)向含有硝酸铝和硝酸银的废液中加入一定量的铁粉,则铁与硝酸银反应生成硝酸亚铁和银,不与硝酸铝反应;反应后所得滤液呈浅绿色,则滤渣中一定含有银,不一定含有铁,滤渣的组成有银或银、铁两种情况;
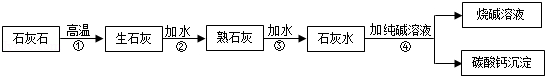
(4)方法2的反应需要加热,能耗较高,而方法2不需要加热,只需加入液体试剂即可。
故答案为:(1)Fe+2HCl=FeCl2+H2↑;
(2)隔绝氧气和水;
(3)2;
(4)能耗较低(合理即可)。
[点评]
本题考查了"金属的化学性质,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。