服务热线
搜题▪组卷
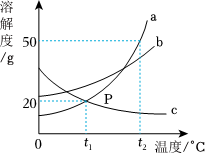
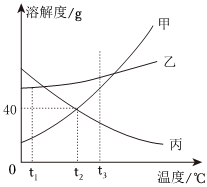 如图,依据甲、乙、丙三种物质的溶解度曲线,回答下列问题:
如图,依据甲、乙、丙三种物质的溶解度曲线,回答下列问题: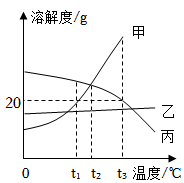 甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题: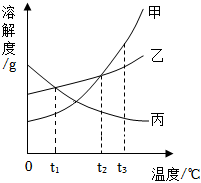 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。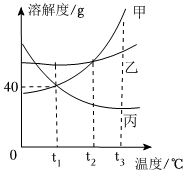 甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。
甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。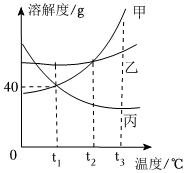 甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。
甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。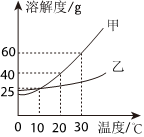 如图是甲、乙两种固体物质的溶解度曲线。据图回答:
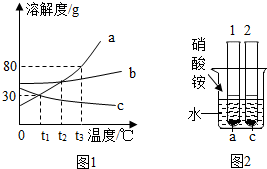
如图是甲、乙两种固体物质的溶解度曲线。据图回答: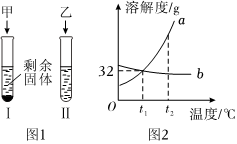 t2℃时,向分别盛有30mL水的Ⅰ、Ⅱ两支试管中分别加入等质量的甲、乙两种固体,充分溶解并恢复原温后,观察到如图1所示的现象。图2是甲、乙两种固体的溶解度曲线,请回答:
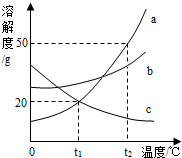
t2℃时,向分别盛有30mL水的Ⅰ、Ⅱ两支试管中分别加入等质量的甲、乙两种固体,充分溶解并恢复原温后,观察到如图1所示的现象。图2是甲、乙两种固体的溶解度曲线,请回答: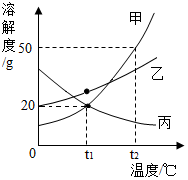 如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.
如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.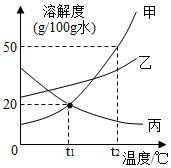 图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。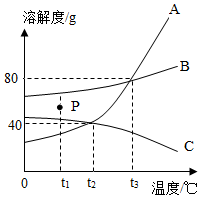


jp@dyw.com
2025-04-07
初中化学 | | 填空题