[考点]
酸的化学性质,碱的通性,中和反应的概念及微观本质,中和反应与复分解反应的关系,
[答案]
(1)BC;
(2)①紫色石蕊;②Na2SO4;③2、5、6;4。
[解析]
解:(1)A.中和反应是酸和碱反应生成盐和水,有盐和水生成的反应不一定是中和反应,如CO2+2NaOH=Na2CO3+H2O,不属于中和反应,故错误;
B.中和反应是酸和碱反应生成盐和水,符合两种化合物相互交换成分生成另外两种化合物的反应特点,所以中和反应一定属于复分解反应,故正确;
C.碱是指电离时生成的阴离子全部是氢氧根离子的化合物,酸是指电离时生成的阳离子全部是氢离子的化合物;所以酸和碱中一定含有氢元素,故正确;
D.碱不一定能使所有酸碱指示剂变色,如氢氧化铜等难溶性的碱不能使酸碱指示剂变色,故错误;
故选:BC;
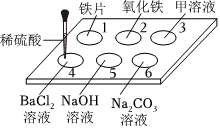
(2)①稀硫酸显酸性,能使紫色石蕊溶液变红色,所以孔穴3中溶液变红,则甲溶液是紫色石蕊溶液;
②无色酚酞溶液遇碱性溶液变红色,遇酸性和中性溶液不变色,孔穴5中氢氧化钠和硫酸反应生成硫酸钠和水,实验结束后向孔穴5中滴加无色酚酞溶液,无明显现象,说明溶液呈中性或酸性,则溶液中一定含有生成的硫酸钠,可能含有硫酸,则加入酚酞溶液前溶液中一定存在的溶质是反应生成的硫酸钠(Na2SO4);
③孔穴1铁和稀硫酸反应生成硫酸亚铁和氢气;孔穴2氧化铁和稀硫酸反应生成硫酸铁和水;孔穴4氯化钡和稀硫酸反应生成硫酸钡沉淀和氯化氢;孔穴5氢氧化钠和稀硫酸反应生成硫酸钠和水;孔穴6碳酸氢钠和稀硫酸反应生成硫酸钠、二氧化碳和水,孔穴1~6中(除孔穴3外)能生成“水”的孔穴有2、5、6;酸具有通性是因为都有氢离子,酸能与酸碱指示剂、活泼金属、金属氧化物、碱、某些盐等反应;孔穴5氢氧化钠和稀硫酸反应生成硫酸钠和水,体现出酸能与碱反应;孔穴6碳酸氢钠和稀硫酸反应生成硫酸钠、二氧化碳和水,体现出酸能跟某些盐反应;而孔穴4氯化钡和稀硫酸反应生成硫酸钡沉淀和氯化氢,实质上是硫酸根离子和钡离子结合生成硫酸钡沉淀,没有体现酸的化学通性,故孔穴4~6中没有体现酸的化学通性的是4。
故答案为:
(1)BC;
(2)①紫色石蕊;②Na2SO4; ③2、5、6;4。
[点评]
本题考查了"酸的化学性质,碱的通性,中和反应的概念及微观本质,中和反应与复分解反应的关系,",属于"综合题",熟悉题型是解题的关键。
 酸碱盐在生产、生活中有着广泛的应用。
酸碱盐在生产、生活中有着广泛的应用。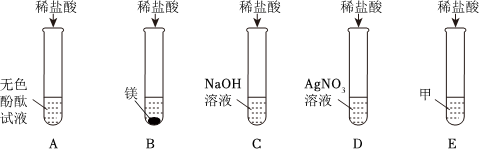
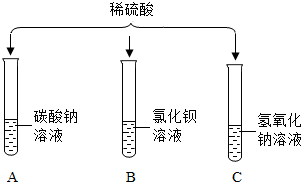
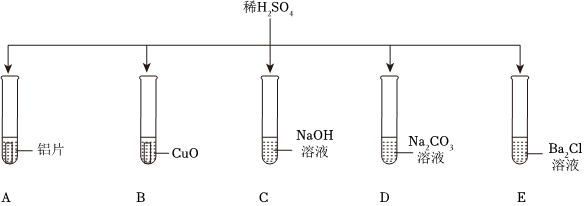
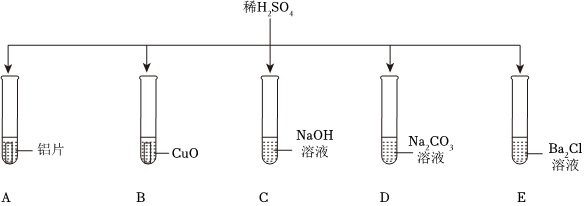
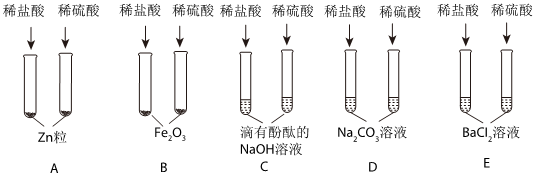
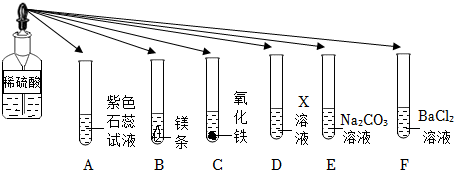
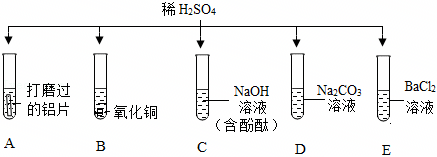
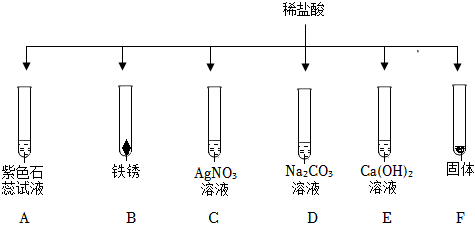
 如图所示,稀硫酸能与相连的物质发生化学反应。
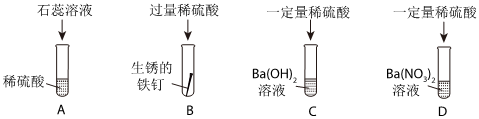
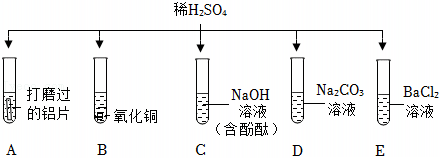
如图所示,稀硫酸能与相连的物质发生化学反应。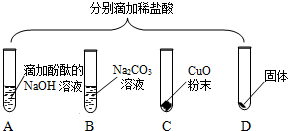 为验证“酸的化学通性”,某班同学在实验室进行如图实验。请分析并回答相关问题:
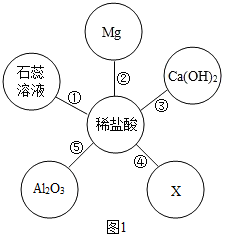
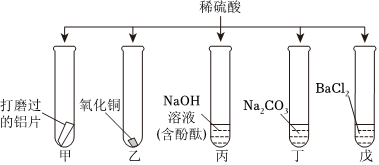
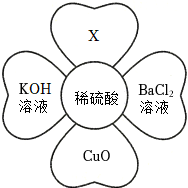
为验证“酸的化学通性”,某班同学在实验室进行如图实验。请分析并回答相关问题: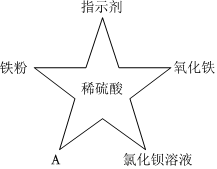 五星红旗闪耀奥运赛场,小王同学复习酸的化学性质时构建了硫酸“五角星图”,其中五个顶角表示与硫酸发生化学反应的五种不同类别的物质。
五星红旗闪耀奥运赛场,小王同学复习酸的化学性质时构建了硫酸“五角星图”,其中五个顶角表示与硫酸发生化学反应的五种不同类别的物质。