[解析]
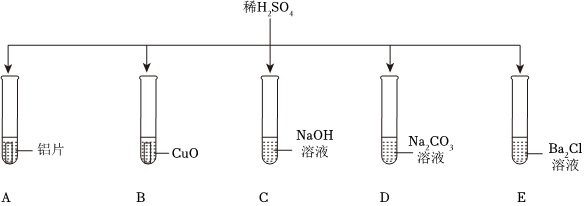
解:(1)A烧杯中是氧化铜(CuO)与稀硫酸(H2SO4)发生反应生成硫酸铜(CuSO4)、水(H2O),化学方程式为:CuO+H2SO4=CuSO4+H2O;
(2)B烧杯中是A烧杯反应后的产物硫酸铜与氯化钡溶液发生反应是CuSO4+BaCl2=BaSO4↓+CuCl2,观察到的现象是:有白色沉淀生成;
(3)①C烧杯中刚开始无明显现象,说明先发生的反应是H2SO4+2NaOH=Na2SO4+2H2O,则B烧杯中稀硫酸有剩余,A烧杯中稀硫酸也一定有剩余,则A烧杯中一定没有固体剩余,①合理;
②B烧杯中发生反应CuSO4+BaCl2=BaSO4↓+CuCl2,反应后生成的氯化铜(CuCl2)一定存在于溶液中,A 烧杯中不一定生成硫酸铜,且B烧杯中稀硫酸有剩余,则B烧杯中所得溶液的溶质一定有CuCl2、H2SO4,②正确;
③C烧杯中,一开始加入氢氧化钠溶液时,氢氧化钠先与剩余的稀硫酸发生中和反应生成硫酸钠和水,消耗了酸性的硫酸,溶液酸性减弱,pH变大。当硫酸反应完后,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,所以整个过程中C烧杯中溶液的pH是变大的,③合理;
故选:①②③;
(4)根据元素守恒原理,A烧杯中氧化铜(CuO)中的铜元素,经过一系列反应后最终全部转化到 C 烧杯生成的氢氧化铜[Cu(OH)2]沉淀中。氧化铜(CuO)的相对分子质量为64+16=80,氢氧化铜[Cu(OH)2]的相对分子质量为64+(16+1)×2=98,所以A中氧化铜固体质量小于C中生成氢氧化铜沉淀的质量,另外,反应过程中还会生成BaSO4沉淀,所以C烧杯产生沉淀的质量与反应前A烧杯中固体的质量关系是 A<C。
故答案为:(1)CuO+H2SO4=CuSO4+H2O;
(2)有白色沉淀生成;
(3)①②③;
(4)<。
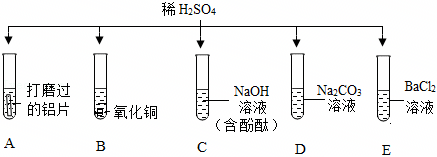
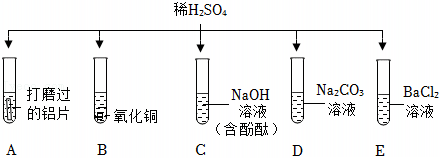
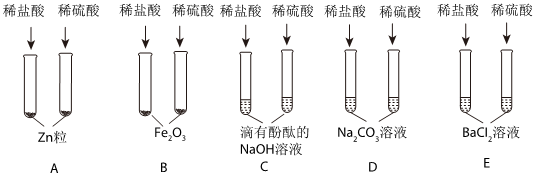
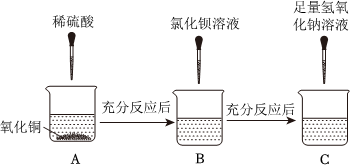 为验证酸碱盐和氧化物的性质与转化,某同学设计如下实验。
为验证酸碱盐和氧化物的性质与转化,某同学设计如下实验。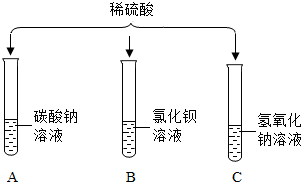
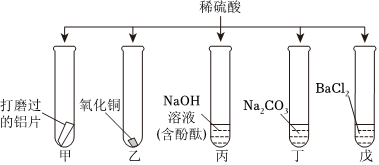
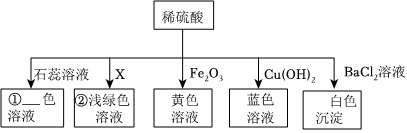
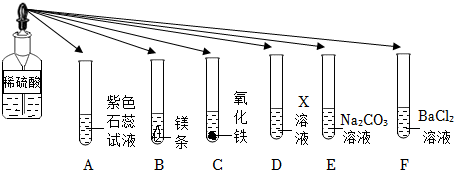
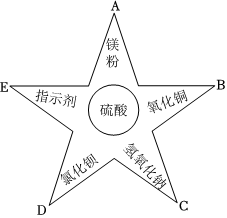 小乐同学复习酸的化学性质时,构建了硫酸的“五角星图”,其中五个顶角表示能与硫酸发生化学反应的五类物质。
小乐同学复习酸的化学性质时,构建了硫酸的“五角星图”,其中五个顶角表示能与硫酸发生化学反应的五类物质。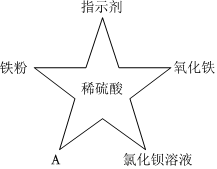 五星红旗闪耀奥运赛场,小王同学复习酸的化学性质时构建了硫酸“五角星图”,其中五个顶角表示与硫酸发生化学反应的五种不同类别的物质。
五星红旗闪耀奥运赛场,小王同学复习酸的化学性质时构建了硫酸“五角星图”,其中五个顶角表示与硫酸发生化学反应的五种不同类别的物质。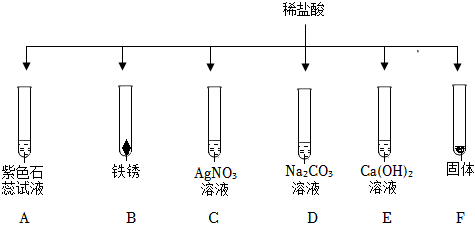
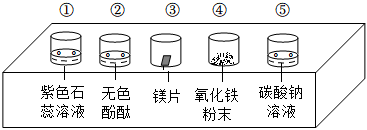
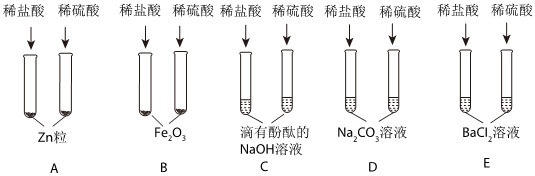
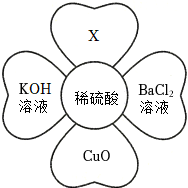 如图所示,稀硫酸能与相连的物质发生化学反应。
如图所示,稀硫酸能与相连的物质发生化学反应。