服务热线
搜题▪组卷
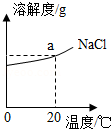
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | |
| 溶解度/g | NaCl | 36. | 36.3 | 36.6 | 37. | 37.3 | 37.8 | 38 | 38.5 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110. | 138 | 169 | 202 | |
| 温度/℃ | 10 | 20 | 40 | 60 |
| 溶解度/g | 21 | 32 | 64 | 110 |
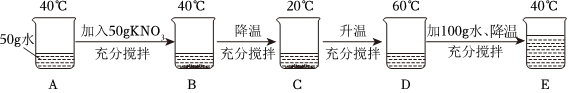

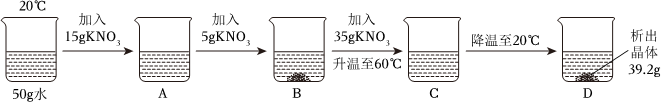

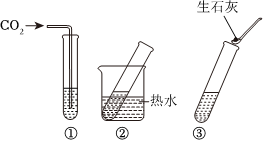
| 组别 物质质量 |
A | B | C | D | E |
| NaCl晶体质量/g | 5 | 15 | 20 | 30 | 40 |
| 所得溶液质量/g | 105 | 115 | X | 130 | 136 |
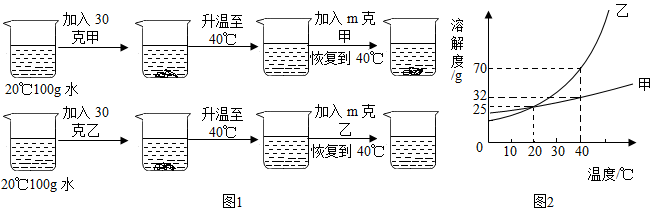
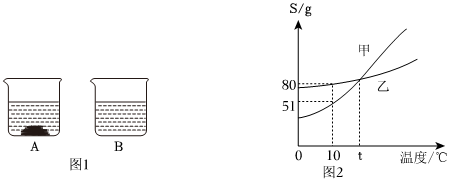
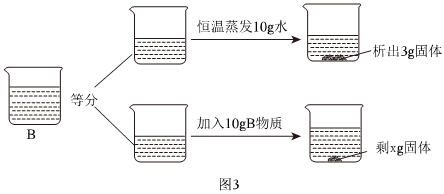
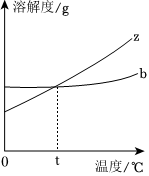
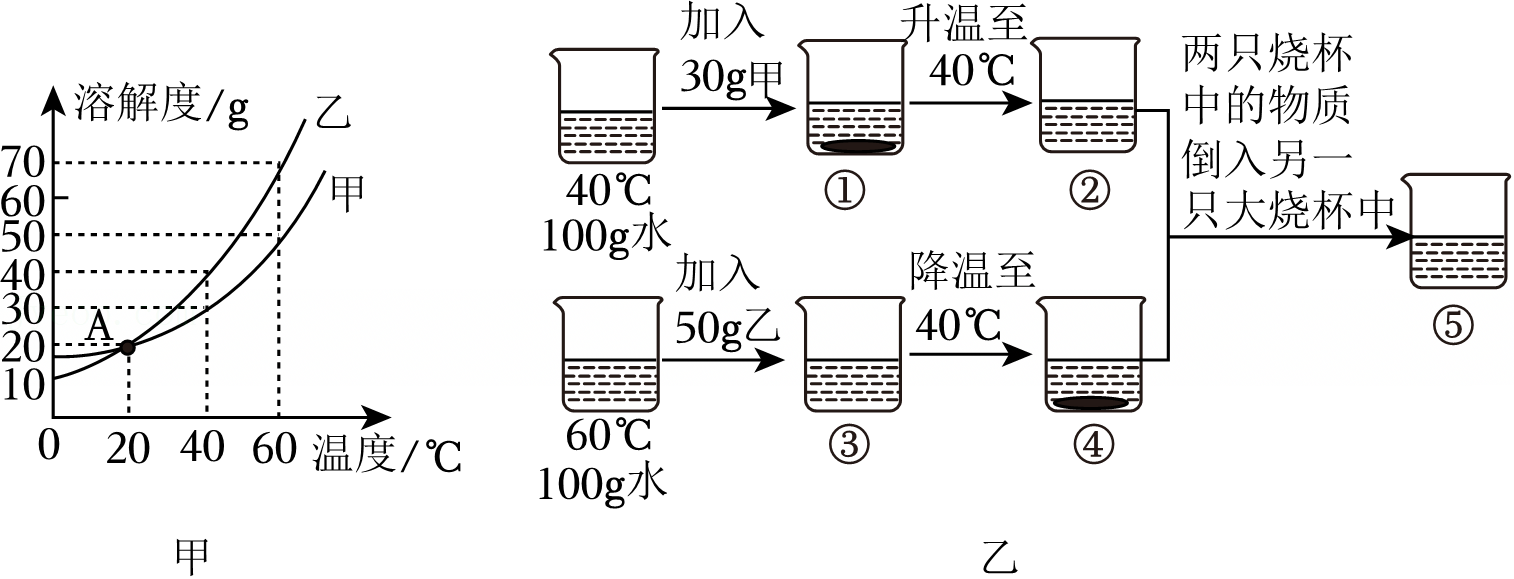
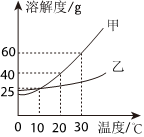 如图是甲、乙两种固体物质的溶解度曲线。据图回答:
如图是甲、乙两种固体物质的溶解度曲线。据图回答: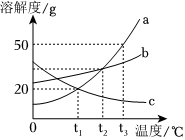
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 27.6 | 31.0 | 36.0 | 37.0 | 37.3 | 37.3 | 37.8 | |

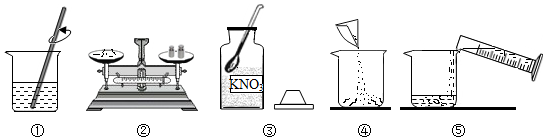
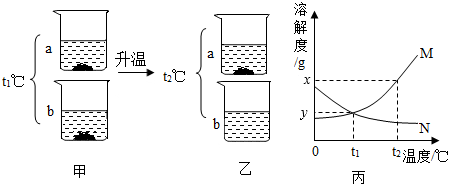
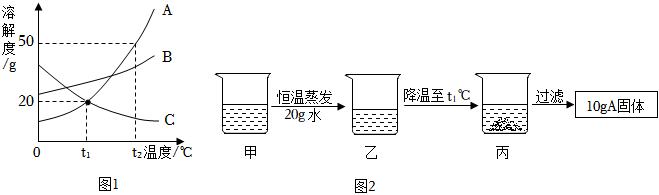
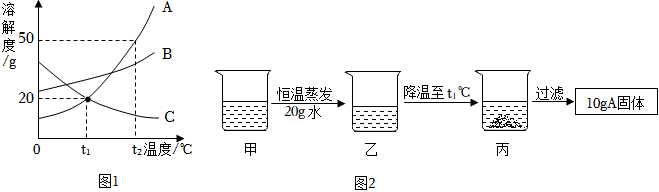
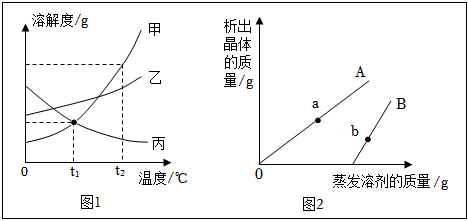
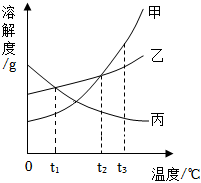 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。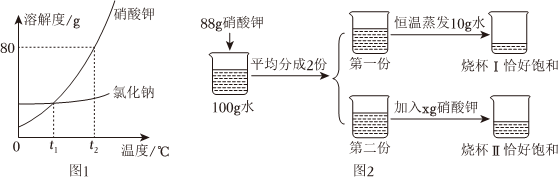

bq@dyw.com
2025-03-21
初中化学 | | 填空题