服务热线
搜题▪组卷
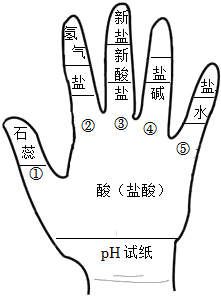 构建模型和构建知识网络是化学学习中重要的学习方法,小雷同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
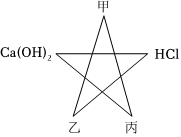
构建模型和构建知识网络是化学学习中重要的学习方法,小雷同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题: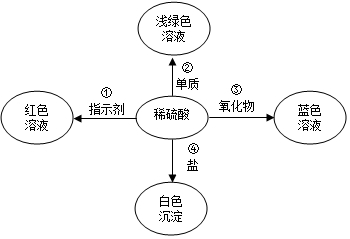 化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化,稀硫酸与不同的物质反应呈现出不同的颜色.
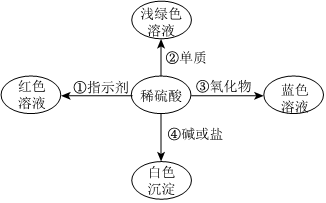
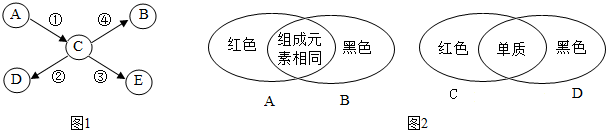
化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化,稀硫酸与不同的物质反应呈现出不同的颜色.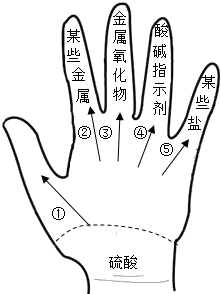 某同学利用左手构建的酸的性质和知识网络,如图所示,(箭头表示稀盐酸能与指向的物质反应),请结合图示,回答下列问题:
某同学利用左手构建的酸的性质和知识网络,如图所示,(箭头表示稀盐酸能与指向的物质反应),请结合图示,回答下列问题: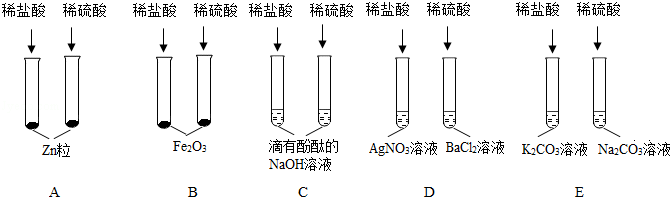
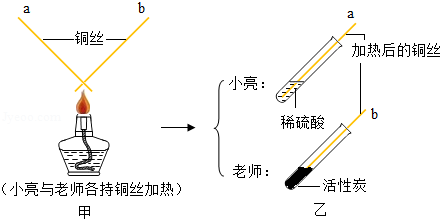
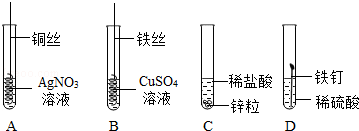
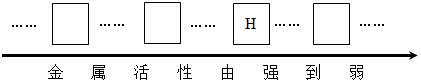
 小丽学习酸、碱的知识后,构建了有关酸、碱与甲、乙、丙三种初中常见物质之间的反应关系图,图中连线两端的物质均能发生反应,其中甲为黑色固体单质,乙、丙为氧化物。请回答:
小丽学习酸、碱的知识后,构建了有关酸、碱与甲、乙、丙三种初中常见物质之间的反应关系图,图中连线两端的物质均能发生反应,其中甲为黑色固体单质,乙、丙为氧化物。请回答: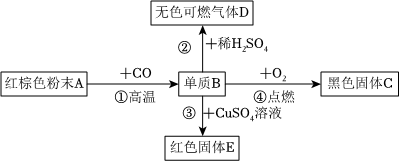
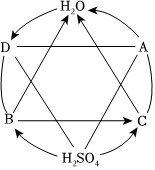 如图是初中化学几种常见物质之间的反应关系图。已知B和C的物质类别相同。A和D的反应可用于制取烧碱。H2O→D的反应会放出热量。图中“—”表示相连的两种物质能反应,“→”表示两端的物质通过一步反应能转化。
如图是初中化学几种常见物质之间的反应关系图。已知B和C的物质类别相同。A和D的反应可用于制取烧碱。H2O→D的反应会放出热量。图中“—”表示相连的两种物质能反应,“→”表示两端的物质通过一步反应能转化。
yy@dyw.com
2024-02-12
初中化学 | 九年级上 | 填空题