[答案]
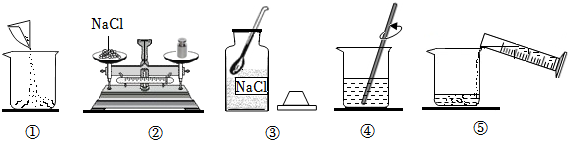
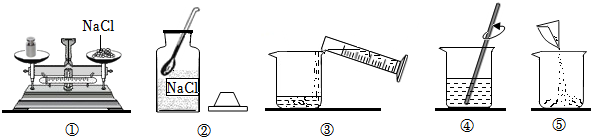
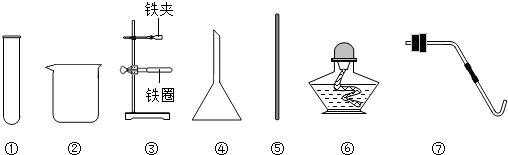
(1)③②①⑤④;
(2)广口瓶;减少氯化钠的质量,直至天平平衡;
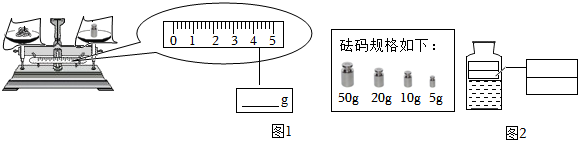
(3)100;凹液面的最低处;
(4)搅拌,加快溶解速率。
[解析]
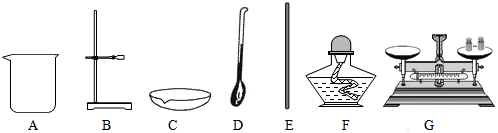
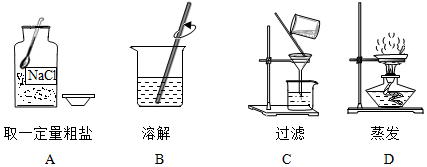
解:(1)配制100g溶质质量分数为25%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故正确的操作顺序是③②①⑤④。
(2)图③中盛放氯化钠固体的仪器是广口瓶;称量氯化钠时,在往左盘慢慢加入氯化钠的过程中,指针偏左,说明药品的质量大于砝码的质量,接下来的操作是
减少氯化钠的质量,直至天平平衡。
(3)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为25%的氯化钠溶液,需氯化钠的质量=100g×25%=25g;溶剂质量=溶液质量﹣溶质质量,则所需水的质量=100g﹣25g=75g(合75mL),量筒量程的选择,应遵循“大而近”的原则,应用规格为100mL的量筒量取水的体积。读数时视线要与量筒内凹液面的最低处保持水平。
(4)溶解操作中,需要使用玻璃棒,玻璃棒的作用是搅拌,加快溶解速率。
故答案为:
(1)③②①⑤④;
(2)广口瓶;减少氯化钠的质量,直至天平平衡;
(3)100;凹液面的最低处;
(4)搅拌,加快溶解速率。
[点评]
本题考查了"浓溶液稀释配制一定质量分数溶液,",属于"基础题",熟悉题型是解题的关键。