[考点]
生铁和钢,金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式,
[解析]
解:(1)生铁的主要成分是铁,还含有一些杂质,属于混合物;
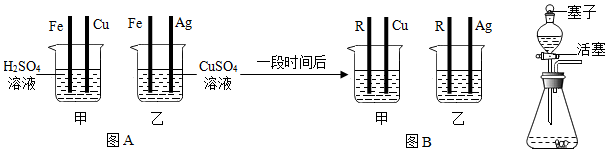
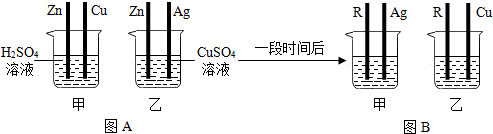
(2)①由图A所示可知,将四根金属丝同时插入烧杯中,乙中Fe和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
②一段时间后,将烧杯中铁丝替换为R进行实验,由于甲中出现气泡,说明了R在金属活动性顺序表中,位于氢的前边,由于乙中无明显现象,烧杯乙中的溶质是FeSO4,说明R的活泼性小于铁,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为:Fe>R>Cu>Ag.
故答案为:(1)混合物;(2)①Fe+CuSO4═FeSO4+Cu;②Fe>R>Cu>Ag.
[点评]
本题考查了"生铁和钢,金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式,",属于"难典题",熟悉题型是解题的关键。