[考点]
金属的物理性质及用途,金属的化学性质,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式,
[解析]
解:(1)铁锅可用来炒菜,利用了金属的导热性.
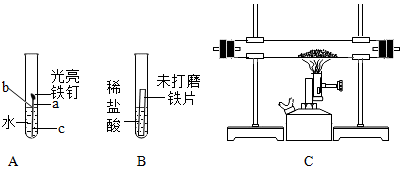
(2)某企业仓库里长期堆放的机械设备的锈迹斑斑,其原因是铁长期与空气中水和氧气接触,发生了缓慢氧化所致.
(3)小明将设备上的一枚生锈的螺丝放入足量的稀硫酸中,发现铁锈逐渐消失,溶液变成黄色,一段时间后,又观察到铁钉表面有大量气泡产生,溶液变黄的原因是氧化铁与硫酸反应生成了硫酸铁和水,化学反应式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
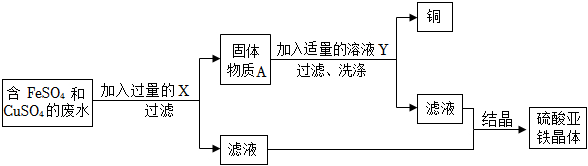
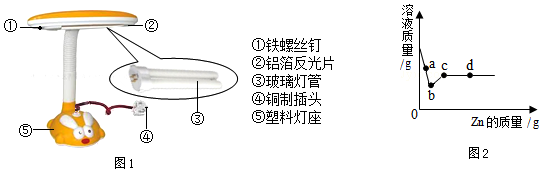
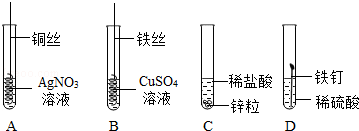
(4)A、由于浓硫酸具有强氧化性,与铁反应不能生成氢气,故A错误;
B、若X为金属单质,则X的活动性一定比铁若,故B错误;
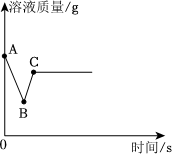
C、若溶液甲是硫酸镁溶液,铁不与硫酸镁反应,则溶液质量不变.故C错误;
D、若溶液甲是硝酸银和硝酸铜的混合溶液,当硝酸银完全反应后,则溶液乙可能只含有Cu2+和Fe2+两种阳离子.故D正确.
故答案为:(1)导热;(2)水和氧气;(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;(4)D.
[点评]
本题考查了"金属的物理性质及用途,金属的化学性质,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式,",属于"压轴题",熟悉题型是解题的关键。
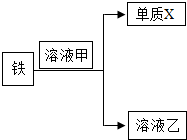 钢铁是生产、生活中使用非常广泛的金属.
钢铁是生产、生活中使用非常广泛的金属.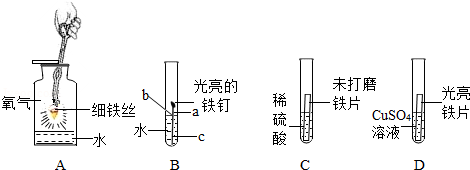
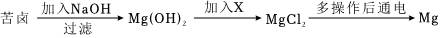
 金属的利用史成就卓越,是劳动人民生产与生活智慧的结晶。
金属的利用史成就卓越,是劳动人民生产与生活智慧的结晶。