服务热线
搜题▪组卷
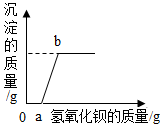 R溶液可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。回答下列问题。
R溶液可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。回答下列问题。
 |
 |
 |
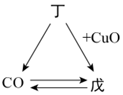 |
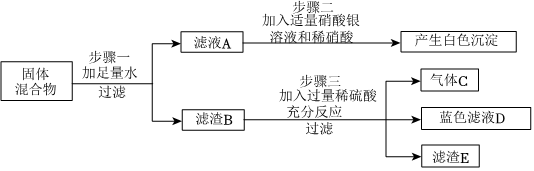
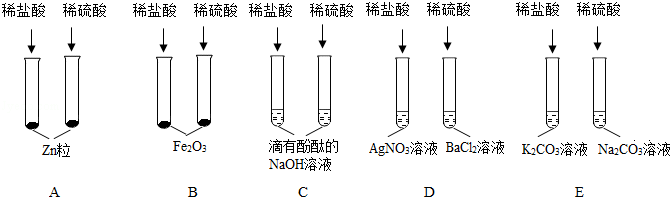
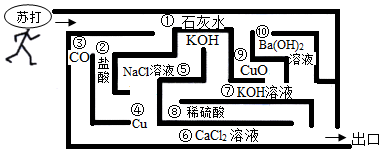
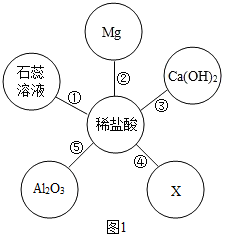
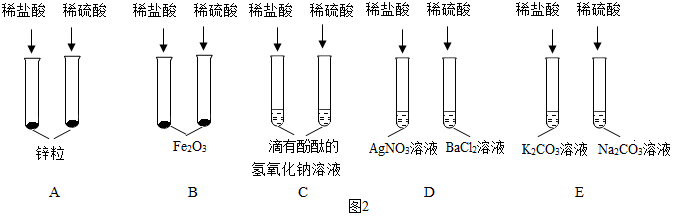
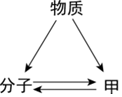
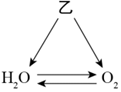
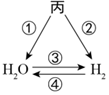
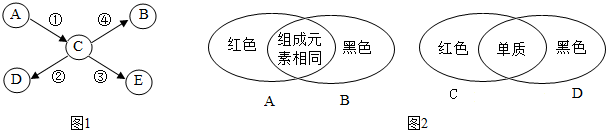
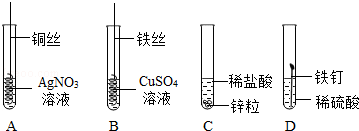
| (1)题图 | (2)题图 | (3)题图 | (4)题图 |

ty@dyw.com
2017-04-18
初中化学 | | 填空题