[解析]
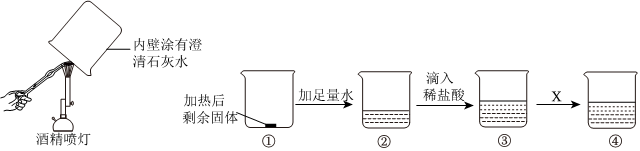
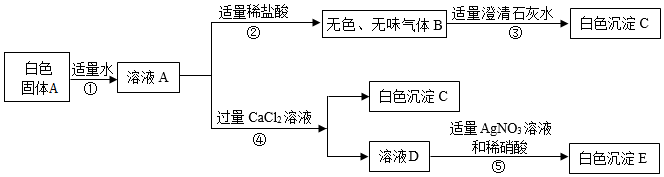
解:(1)B是二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;
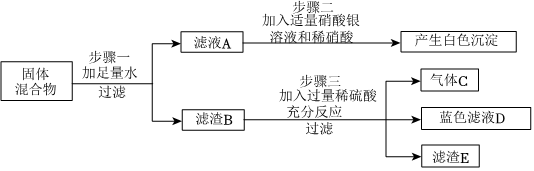
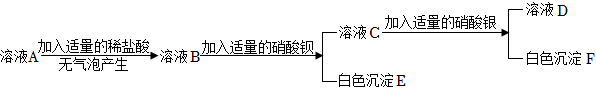
(2)碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,因此溶液D中有氯化钠和氯化钙,阳离子是钠离子和钙离子;故答案为:Na+、Ca2+;
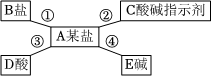
(3)A是一种常见的钠盐,便取了少许固体A先进行加热,发现它没有明显变化,说明A受热不易分解;碳酸钠溶液与盐酸反应生成氯化钠和水和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,因此A是碳酸钠,B是二氧化碳,C是碳酸钙;故答案为:Na2CO3;
(4)根据步骤⑤中的实验现象,小令同学分析并推断出溶液A中还混有NaCl,我不同意他的观点,因为第④步就生成氯化钠,要想分析推断出溶液A中是否还混有NaCl,需要定量计算;故答案为:不同意;因为第④步就生成氯化钠,要想分析推断出溶液A中是否还混有NaCl,需要定量计算。

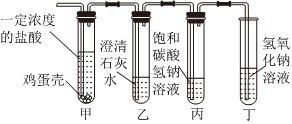
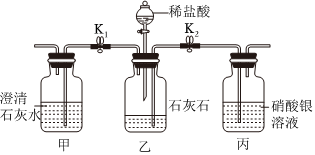
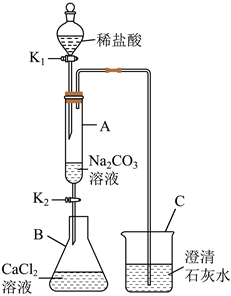 用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。
用如图装置完成下列实验(夹持仪器已省略,K1、K2均关闭)。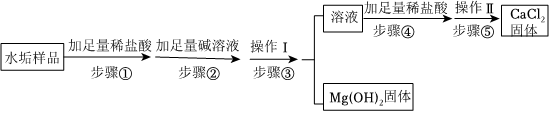
 ?
?