[考点]
常用气体的发生装置和收集装置与选取方法,玻璃棒在过滤中的作用,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
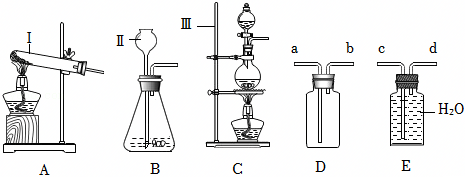
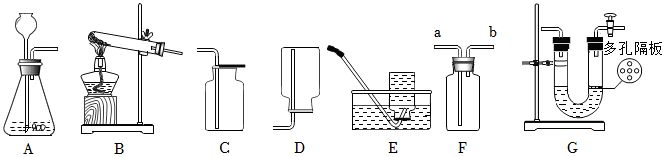
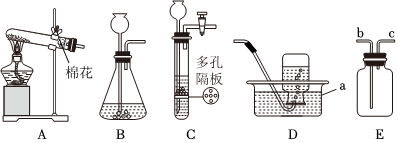
(2)试管;a;
(3)引流;
(4)AB。
[解析]
解:(1)实验室制取CO2的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
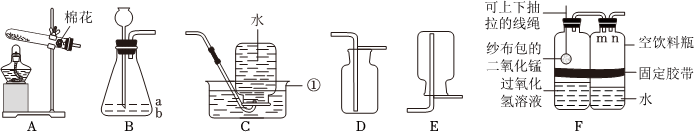
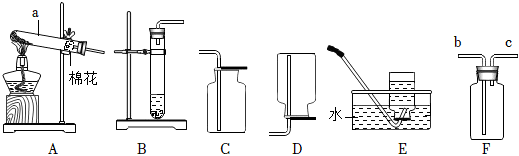
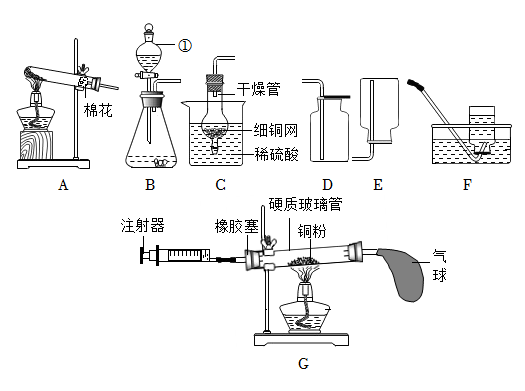
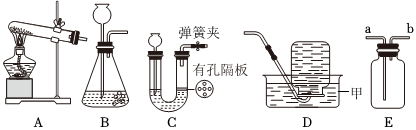
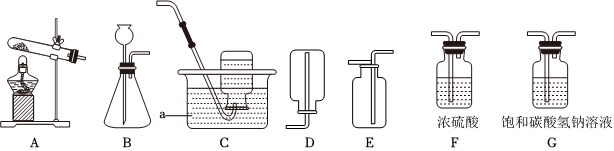
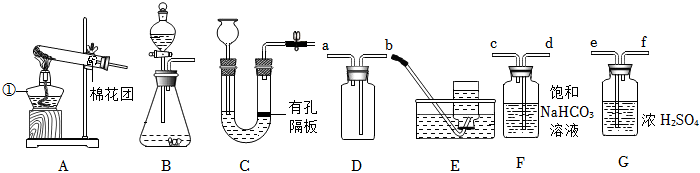
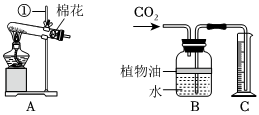
(2)由图可知,仪器Ⅰ的名称是试管;氯气的密度比空气大,用D装置收集Cl2时,Cl2应从a管口进入瓶中。
(3)用A装置制取氧气后,从剩余固体中分离出MnO2的实验步骤有溶解、过滤、洗涤和干燥。过滤时玻璃棒的作用是引流。
(4)A、制取CO2需要固液常温型装置,制取Cl2需要液体加热型装置,二者的发生装置不同,故选项分析不正确;
B、由制取氯气的反应MnO2+4HCl(浓)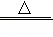 MnCl2+Cl2↑+2H2O可知,制取Cl2的反应中MnO2是反应物,不是催化剂,故选项分析不正确;
C、氧气的密度比水小,则用E装置收集O2时,O2应从d管导入,故选项分析正确;
故选:AB。
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)试管;a;
(3)引流;
(4)AB。
MnCl2+Cl2↑+2H2O可知,制取Cl2的反应中MnO2是反应物,不是催化剂,故选项分析不正确;
C、氧气的密度比水小,则用E装置收集O2时,O2应从d管导入,故选项分析正确;
故选:AB。
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)试管;a;
(3)引流;
(4)AB。
[点评]
本题考查了"常用气体的发生装置和收集装置与选取方法,玻璃棒在过滤中的作用,书写化学方程式、文字表达式、电离方程式,",属于"典型题",熟悉题型是解题的关键。