[考点]
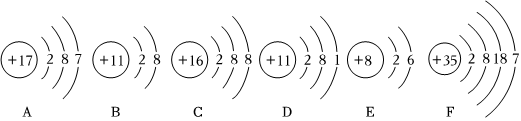
金属活动性顺序及其应用,有关元素化合价的计算,根据质量守恒定律判断物质的化学式,
[解析]
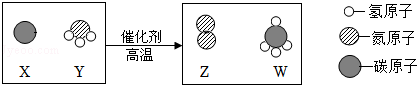
解:(1)根据反应的化学方程式可知,反应物中铁、氧、钾、氢原子个数分别为2、7、4、4,反应后的生成物中铁、氧、钾、氮、氢原子个数分别为2、16、7、3、4,根据反应前后原子种类、数目不变,则3X中含有3个钾原子、3个氮原子和9个氧原子,则每个X分子由1个钾原子、1个氮原子和3个氧原子构成,则物质X的化学式为KNO3.
钾元素显+1价,氧元素显﹣2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(﹣2)×4=0,则x=+6价.
故答案为:KNO3;+6.
(2)①根据反应Cl2+2NaBr═2NaCl+Br2,得出Cl2>Br2;根据反应I2+Na2S═2NaI+S↓,得出I2>S;
根据反应Br2+2KI═2KBr+I2,得出Br2>I2.
故填:Cl2>Br2>I2>S;
②根据非金属活动性规律:Cl2>Br2>I2>S,可知Br2的活动性比I2强,因此单质I2不能把Br从其盐溶液中置换出来,所以反应I2+2KBr═2KI+Br2不正确.
故选:B.
[点评]
本题考查了"金属活动性顺序及其应用,有关元素化合价的计算,根据质量守恒定律判断物质的化学式,",属于"难典题",熟悉题型是解题的关键。
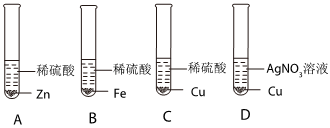
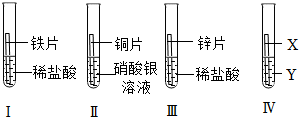
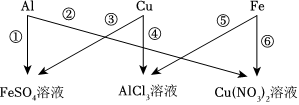 为验证铝、铜、铁的金属活动性顺序,同学们设计了如图所示的6个实验(“→”表示将金属丝加入盐溶液中)。
为验证铝、铜、铁的金属活动性顺序,同学们设计了如图所示的6个实验(“→”表示将金属丝加入盐溶液中)。


 ?
?