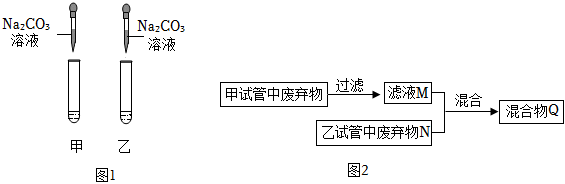
[答案]
(1)A;HCl;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;复分解反应;
(3)Fe2O3+6HCl═2FeCl3+3H2O
[解析]
解:A+B、A+C溶液变红,则A为酚酞试液;B、C显碱性,为氢氧化钙、碳酸钠溶液中的一种,则D为稀盐酸;B+D产生气体,则B为碳酸钠溶液,C为氢氧化钙溶液。
(1)酚酞试液是A;D是稀盐酸,其化学式为HCl。
(2)B与C反应,即碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应。
(3)D在工业上用于焊接钢铁制品,用于除外金属表面的锈,铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O。
故答案为:
(1)A;HCl;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;复分解反应;
(3)Fe2O3+6HCl═2FeCl3+3H2O。
[点评]
本题考查了"酸、碱、盐的鉴别",属于"必考题",熟悉知识点是解题的关键。