服务热线
搜题▪组卷
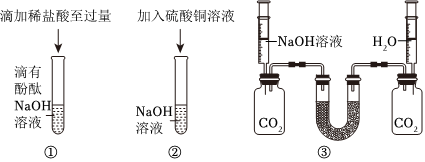
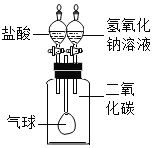
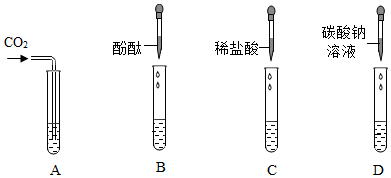
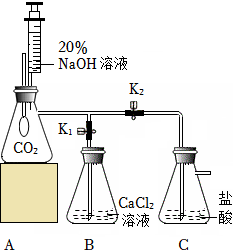 小明同学按图示装置验证CO2和NaOH溶液发生了反应。关闭K1、K2,将20%NaOH溶液注入装满CO2的锥形瓶中,观察到气球胀大。
小明同学按图示装置验证CO2和NaOH溶液发生了反应。关闭K1、K2,将20%NaOH溶液注入装满CO2的锥形瓶中,观察到气球胀大。

lch@dyw.com
2024-12-01
初中化学 | 九年级下 | 填空题