[考点]
金属与氧气的反应,物质的相互转化和制备,反应类型的判定,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)Zn;
(2)CuO+H2SO4=CuSO4+H2O;
(3)A;
(4)H2SO4、CuSO4。
[解析]
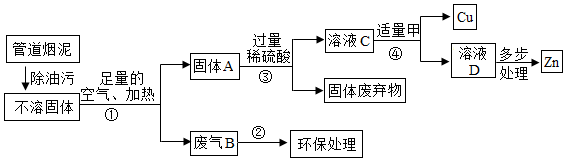
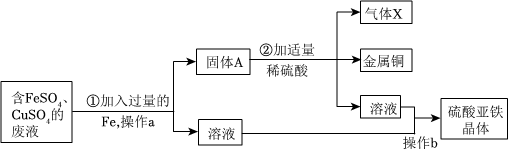
解:(1)步骤①中Zn、Cu转化为ZnO、CuO,S转化为SO2;步骤②中吸收SO2;步骤③将ZnO、CuO转化为ZnSO4、CuSO4;步骤④中可以加入适量的Zn,可以消耗足量的稀硫酸,也可以将CuSO4中Cu置换出来;反应后过滤的滤液中只含有ZnSO4;则试剂甲为Zn;故答案为:Zn;
(2)步骤③中CuO与稀硫酸反应生成硫酸铜与水,化学反应方程式为:CuO+H2SO4=CuSO4+H2O;
(3)A、NaOH能与油污反应生成新物质,则属于化学变化,故选项说法错误;
B、步骤③④均是将固液分离,则主要的操作是过滤,故选项说法正确;
C、废弃中含有SO2,空气中二氧化硫含量过高会导致酸雨的形成,故选项说法正确;
D、步骤①中Zn、Cu与氧气反应属于化合反应;步骤②中为SO2与碱性物质反应;步骤③中ZnO、CuO与稀硫酸反应,属于复分解反应;步骤④中Zn与CuSO4反应、Zn与H2SO4反应属于置换反应,共3中基本反应类型,故选项说法正确;
故答案选:A;
(4)C中溶液的溶质为H2SO4、CuSO4、ZnSO4,则在溶液中加入Mg,金属活动性Mg>Zn>H>Cu,则Mg先与CuSO4反应,生成Cu,再与H2SO4反应产生氢气,最后与ZnSO4反应生成Zn;若向滤渣中加入稀盐酸,观察有气泡产生,则滤渣中一定含有Zn,可能含有Mg,则CuSO4与H2SO4一定被消耗完;故答案为:H2SO4、CuSO4。
[点评]
本题考查了"金属与氧气的反应,物质的相互转化和制备,反应类型的判定,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。

 ?
?