[考点]
合金与合金的性质,金属活动性顺序及其应用,根据质量守恒定律判断物质的化学式,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)耐腐蚀;
(2)SO3;
(3)Fe+CuCl2=FeCl2+Cu。
[解析]
解:(1)合金钢不仅强度大而且还具有很好的耐腐蚀性能;
(2)根据质量守恒定律,反应前后原子的种类、数目不变,反应前Ti、F、H、S、O的原子个数分别为1、4、4、2、8,反应后Ti、F、H、S、O的原子个数分别为1、4、4、0、2,2X中含有2个硫原子和6个氧原子,X的化学式为SO3;
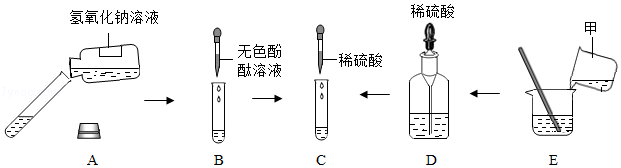
(3)向适量ZnCl2溶液中加入足量铁粉后,无明显现象,说明锌比铁活泼,再加入CuCl2溶液,析出红色固体,溶液由蓝色变成浅绿色,说明铁比铜活泼,即铁与氯化铜反应生成氯化亚铁和铜,反应的化学方程式为Fe+CuCl2=FeCl2+Cu。
故答案为:(1)耐腐蚀;
(2)SO3;
(3)Fe+CuCl2=FeCl2+Cu。
[点评]
本题考查了"合金与合金的性质,金属活动性顺序及其应用,根据质量守恒定律判断物质的化学式,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。

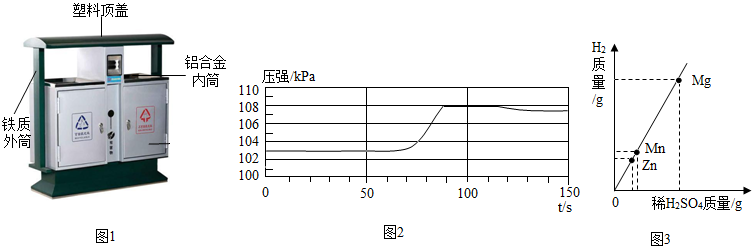 (1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。
(1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。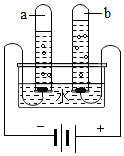 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。
在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。