服务热线
搜题▪组卷
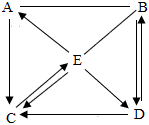
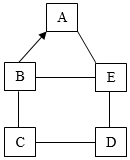 A、B、C、D、E分别是稀硫酸、镁、氢氧化钠溶液、氧化镁及硫酸铜溶液中的一种。如图中“-”表示相连的物质间可以相互反应,“→”表示B在一定条件下可以转化为A。已知C溶液呈蓝色。请回答以下问题:
A、B、C、D、E分别是稀硫酸、镁、氢氧化钠溶液、氧化镁及硫酸铜溶液中的一种。如图中“-”表示相连的物质间可以相互反应,“→”表示B在一定条件下可以转化为A。已知C溶液呈蓝色。请回答以下问题: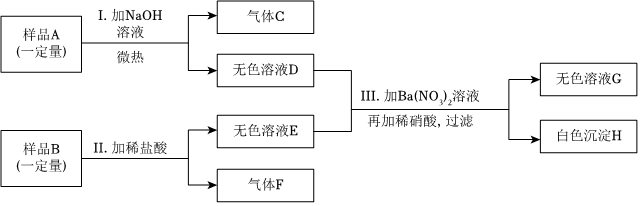
 A~G为实验室中未贴标签的7种溶液。已知7种溶液分别为:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液。
A~G为实验室中未贴标签的7种溶液。已知7种溶液分别为:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液。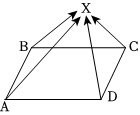
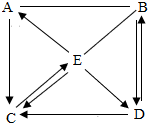 A-E是初中化学常见的物质,其中B是光合作用的原料、C是相对分子质量最小的氧化物,A、E物质类别相同且都属于碱,D是大理石的主要成分,D、B中含有相同的非金属元素。物质间的转化关系如图所示(“—”表示相邻两物质间能发生反应,“→”表示一种物质经一步反应装化为另一科物质,部分反应物、生成物及反应条件已略去)。请回答下列问题。
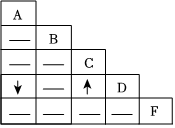
A-E是初中化学常见的物质,其中B是光合作用的原料、C是相对分子质量最小的氧化物,A、E物质类别相同且都属于碱,D是大理石的主要成分,D、B中含有相同的非金属元素。物质间的转化关系如图所示(“—”表示相邻两物质间能发生反应,“→”表示一种物质经一步反应装化为另一科物质,部分反应物、生成物及反应条件已略去)。请回答下列问题。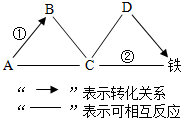 A、B、C、D分别为四种不同类别的化合物,它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),B为大理石主要成分,C由两种元素组成。试推断并回答下列相关问题:
A、B、C、D分别为四种不同类别的化合物,它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),B为大理石主要成分,C由两种元素组成。试推断并回答下列相关问题: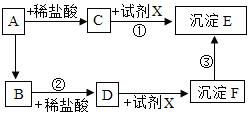 如图所示,A是红棕色固体,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红褐色沉淀。查阅资料可知:反应③是物质F与氧气、水发生的化合反应生成物质E。请回答下列问题:
如图所示,A是红棕色固体,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红褐色沉淀。查阅资料可知:反应③是物质F与氧气、水发生的化合反应生成物质E。请回答下列问题: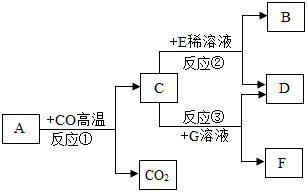
 A-E是初中化学常见的物质,其中B是光合作用的原料、C是相对分子质量最小的氧化物,A、E物质类别相同且都属于碱,D是大理石的主要成分,D、B中含有相同的非金属元素。物质间的转化关系如图所示(“—”表示相邻两物质间能发生反应,“→”表示一种物质经一步反应装化为另一科物质,部分反应物、生成物及反应条件已略去)。请回答下列问题。
A-E是初中化学常见的物质,其中B是光合作用的原料、C是相对分子质量最小的氧化物,A、E物质类别相同且都属于碱,D是大理石的主要成分,D、B中含有相同的非金属元素。物质间的转化关系如图所示(“—”表示相邻两物质间能发生反应,“→”表示一种物质经一步反应装化为另一科物质,部分反应物、生成物及反应条件已略去)。请回答下列问题。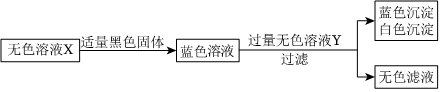
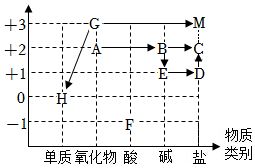 如图是依据物质类别和物质中元素的化合价构建的物质间的转化关系图(“→”表示物质间的转化),已知A~M等9种物质是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种组成的物质。
如图是依据物质类别和物质中元素的化合价构建的物质间的转化关系图(“→”表示物质间的转化),已知A~M等9种物质是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种组成的物质。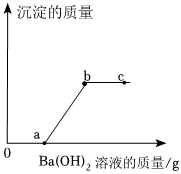 某溶液中溶质可能是HCl、Na2CO3、H2SO4、CuCl2中的一种或多种,为探究溶质的成分,兴趣小组的同学向盛有一定量样品的烧杯中逐滴加入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的变化趋势如图所示。
某溶液中溶质可能是HCl、Na2CO3、H2SO4、CuCl2中的一种或多种,为探究溶质的成分,兴趣小组的同学向盛有一定量样品的烧杯中逐滴加入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的变化趋势如图所示。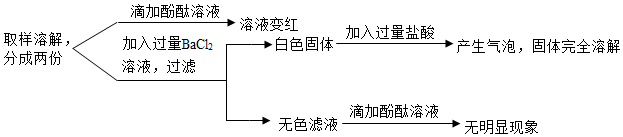
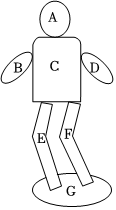 2025年春晚机器人节目的出现不仅是科技与艺术融合的生动体现,也为文化传播、教育发展和未来社会的科技应用提供了重要启示。如图是化学兴趣小组同学利用化学物质构建的机器人模型,其中A~G分别是稀盐酸、氢氧化钙、碳酸钙、氢氧化钠、铁、氧化铜、氯化镁七种物质中的一种。A为大理石的主要成分,B含有两种元素,人体胃液中含有C,相邻的物质之间能发生化学反应(所涉及反应均为初中常见的化学反应),请回答下列问题:
2025年春晚机器人节目的出现不仅是科技与艺术融合的生动体现,也为文化传播、教育发展和未来社会的科技应用提供了重要启示。如图是化学兴趣小组同学利用化学物质构建的机器人模型,其中A~G分别是稀盐酸、氢氧化钙、碳酸钙、氢氧化钠、铁、氧化铜、氯化镁七种物质中的一种。A为大理石的主要成分,B含有两种元素,人体胃液中含有C,相邻的物质之间能发生化学反应(所涉及反应均为初中常见的化学反应),请回答下列问题:
mdt@dyw.com
2021-05-10
初中化学 | | 填空题