[考点]
饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度表格及其作用,
[答案]
(1)硝酸钾;
(2)碳酸钾;
(3)不饱和;32;
(4)B。
[解析]
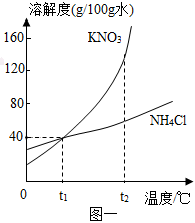
解:(1)通过分析表中的数据可知,两种物质中随温度的升高溶解度变化幅度较大的是硝酸钾;
(2)20℃时,碳酸钾的溶解度大于硝酸钾的溶解度,所以分别将55g两种物质溶于50g水中,所得溶液溶质质量分数较大的是碳酸钾;
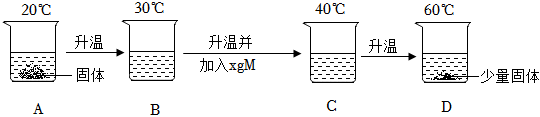
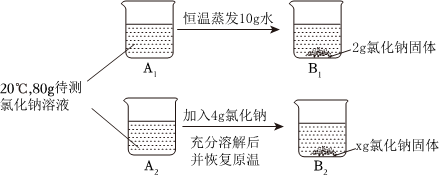
(3)B溶液蒸发10g水,析出的晶体是8.8g,所以B中溶液是不饱和溶液;80g的水在80℃时,溶解的碳酸钾质量是:80g×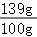 =111.2g,在80℃时,溶解的碳酸钾质量是:80g×
=111.2g,在80℃时,溶解的碳酸钾质量是:80g×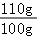 =88g,所以D中x的值是111.2g﹣88g+8.8g=32。
(4)A、20℃时,碳酸钾的溶解度是110g,硝酸钾的溶解度是31.6g,各取5g分别加入到10g水中观察溶解情况,有固体剩余的是是硝酸钾,没有固体剩余的是碳酸钾,故正确;
B、40℃时,取等质量两种溶液降温至20℃,溶液的状态不能确定,所以晶体的析出量也不能确定,故错误;
C、取两种物质的溶液分别加入稀盐酸,碳酸钾和盐酸反应会生成二氧化碳,故正确;
D、取两种物质的溶液分别加入氢氧化钙溶液,碳酸钾和氢氧化钙反应生成会生成碳酸钙沉淀,故正确。
故选:B。
故答案为:(1)硝酸钾;
(2)碳酸钾;
(3)不饱和;32;
(4)B。
=88g,所以D中x的值是111.2g﹣88g+8.8g=32。
(4)A、20℃时,碳酸钾的溶解度是110g,硝酸钾的溶解度是31.6g,各取5g分别加入到10g水中观察溶解情况,有固体剩余的是是硝酸钾,没有固体剩余的是碳酸钾,故正确;
B、40℃时,取等质量两种溶液降温至20℃,溶液的状态不能确定,所以晶体的析出量也不能确定,故错误;
C、取两种物质的溶液分别加入稀盐酸,碳酸钾和盐酸反应会生成二氧化碳,故正确;
D、取两种物质的溶液分别加入氢氧化钙溶液,碳酸钾和氢氧化钙反应生成会生成碳酸钙沉淀,故正确。
故选:B。
故答案为:(1)硝酸钾;
(2)碳酸钾;
(3)不饱和;32;
(4)B。
[点评]
本题考查了"饱和溶液和不饱和溶液,晶体和结晶的概念与现象,固体溶解度表格及其作用,",属于"典型题",熟悉题型是解题的关键。

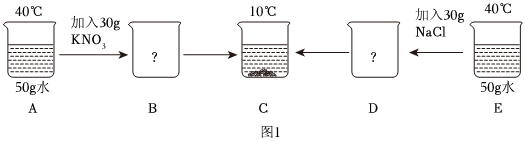
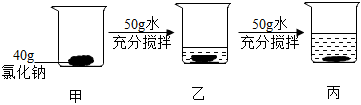
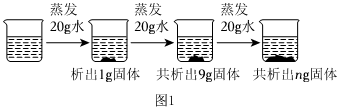
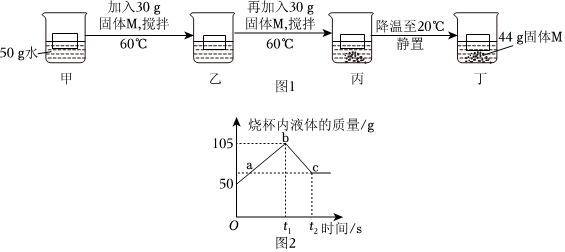
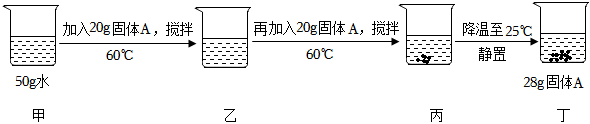
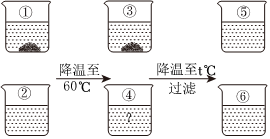 硝酸钾和氯化钠的溶解度如表格所示。80℃时,小明同学将等质量的两种固体分别放入含有100g水的①②烧杯中,接下来进行如图所示实验:
硝酸钾和氯化钠的溶解度如表格所示。80℃时,小明同学将等质量的两种固体分别放入含有100g水的①②烧杯中,接下来进行如图所示实验: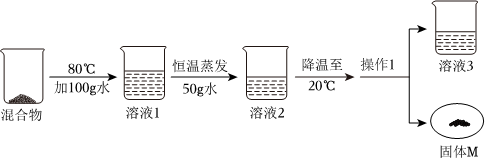
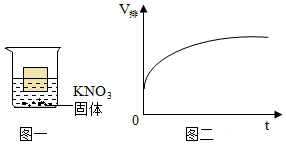
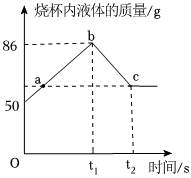
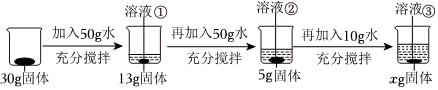
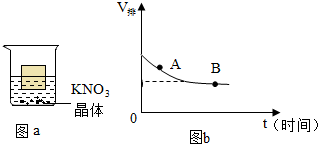
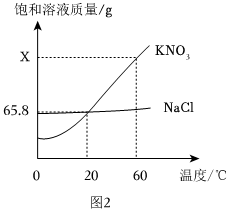
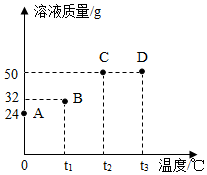 将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得溶液的质量分别如图中A、B、C、D点所示。回答下列问题:(1)0℃时,物质X的溶解度是 。
将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得溶液的质量分别如图中A、B、C、D点所示。回答下列问题:(1)0℃时,物质X的溶解度是 。