服务热线
搜题▪组卷
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37.0 | 37.3 | |
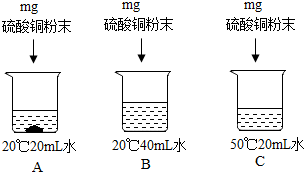
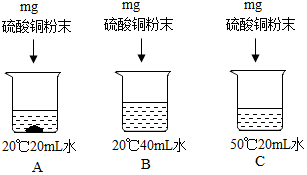
| 温度℃ | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 硝酸钾 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
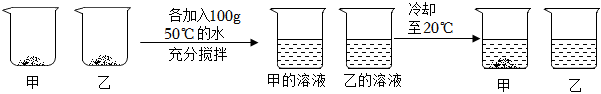
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |

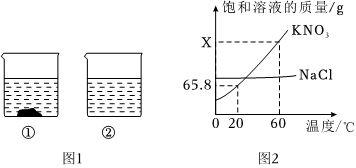
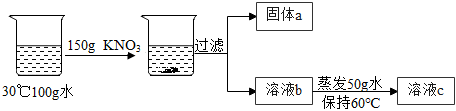
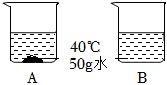 KNO3常用于制造烟火、火柴、肥料等,NaCl是生活中重要的调味品。下表是KNO3、NaCl在不同温度下的部分溶解度数据:
KNO3常用于制造烟火、火柴、肥料等,NaCl是生活中重要的调味品。下表是KNO3、NaCl在不同温度下的部分溶解度数据:| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | |
| 溶解度 (g/100g水) |
NaCl | 35.7 | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.9 | 21.2 | 31.6 | 61.3 | 106 | 167 | |
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | X | 45.8 | 63.9 | 85.5 | 110 | |
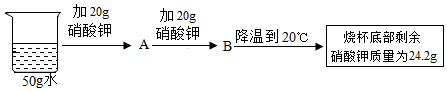
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |

| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
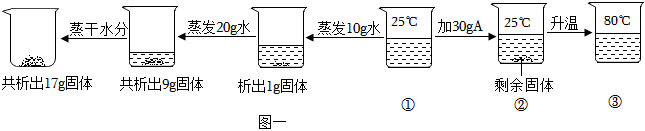
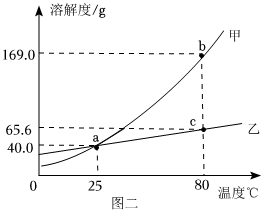
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KCl | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | l10 | l38 | 169 | |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
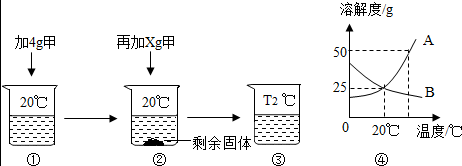
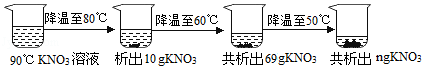
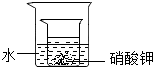 如表是硝酸钾固体在不同温度时的溶解度。
如表是硝酸钾固体在不同温度时的溶解度。| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 |
| 溶剂溶质 | 10mL水 | 10mL汽油 |
| 高锰酸钾(1~2粒) | 全部溶解 | 几乎不溶解 |
| 碘(1~2粒) | 几乎不溶解 | 全部溶解 |

gyy@dyw.com
2023-04-05
初中化学 | | 填空题