[解析]
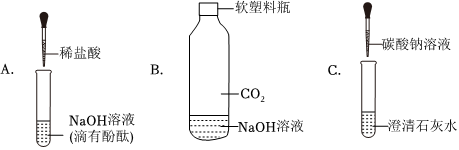
解:(1)酚酞遇碱性溶液变红色,遇中性或酸性溶液不变色,滴有酚酞的氢氧化钠溶液显红色,随着盐酸的滴入,溶液由红色变无色,说明氢氧化钠被消耗,即氢氧化钠与盐酸发生了反应;
(2)B中二氧化碳和氢氧化钠反应生成碳酸钠和水,装置内气体减小 压强减小,塑料瓶变瘪,化学方程式为:CO2+2NaOH=Na2CO3+H2O;
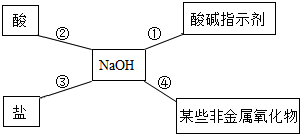
(3)A稀盐酸和氢氧化钠反应生成氯化钠和水,体现了碱能与酸反应生成盐和水;
B二氧化碳和氢氧化钠反应生成碳酸钠和水,体现了碱能与非金属氧化物反应生成盐和水;
C碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,该反应的实质是钙离子和碳酸根离子结合生成碳酸钙沉淀的反应,不能体现碱的通性;
因此,实验A、B、C中不能体现碱的通性的是C;
(4)A稀盐酸和氢氧化钠反应生成氯化钠和水,反应后A试管中一定含有氯化钠、酚酞;
B二氧化碳和氢氧化钠反应生成碳酸钠和水,反应后B试管中一定含有碳酸钠;
C碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,反应后C试管中一定含有碳酸钙沉淀和氢氧化钠;
实验结束后,兴趣小组的同学将A、B、C三个实验后的所有物质都倒入废液缸,发现冒气泡、沉淀消失(盐酸和碳酸钙反应生成氯化钙、二氧化碳和水)并得到无色溶液(溶液中不存在碳酸钠和氢氧化钠,即碳酸钠和盐酸反应生成氯化钠、二氧化碳和水,氢氧化钠和盐酸反应生成氯化钠和水),即A中盐酸过量,则该无色溶液中除指示剂外,一定含有的溶质是氯化钠和氯化钙,化学式为CaCl2、NaCl。
故答案为:(1)溶液由红色变无色。
(2)CO2+2NaOH=Na2CO3+H2O。
(3)C。
(4)NaCl和CaCl2。