服务热线
搜题▪组卷
| 选项 | 物质 | 主要实验操作 |
| A | 鉴别氧化铜和二氧化锰 | 观察颜色 |
| B | 除去O2中混有的少量水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C | 检验Na2SO4溶液中是否含有H2SO4 | 取样,滴加氯化钡溶液,观察现象 |
| D | 分离KNO3和Ba(NO3)2的混合溶液 | 先加入过量的碳酸钠溶液,搅拌、静置、过滤、洗涤,再分别向滤液、滤渣中加入适量的稀硝酸,搅拌 |
A.该实验是将氧化铜逐渐加入稀盐酸中
B.n点和m点对应溶液中铜元素质量不相等
C.n点和m点对应溶液蒸发结晶后得到的固体成分相同
D.该曲线不能反映溶液中溶剂质量随时间的变化关系
A.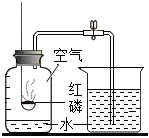
测得空气中氧气的体积分数偏小,可能是止水夹没有夹紧
B.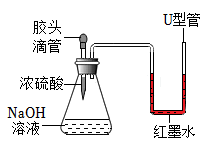
向锥形瓶中滴入浓硫酸后U形管左侧液面降低,说明氢氧化钠和硫酸反应放热
C.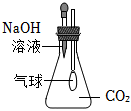
向锥形瓶中滴入NaOH溶液后,气球变大,不能证明NaOH与CO2发生反应
D.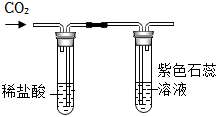
紫色石蕊溶液变红,证明CO2与水反应生成了碳酸
| 待鉴别物质 | 鉴别方法1 | 鉴别方法2 | |
| A | 氧气,二氧化碳 | 用燃着的木条 | 通入NaOH溶液 |
| B | 黄铜,黄金 | 加入硝酸银溶液 | 比较硬度 |
| C | 铝粉,银粉 | 观察颜色 | 加入稀盐酸 |
| D | 氢气,一氧化碳 | 点燃,观察火焰颜色 | 在加热状态下,观察是否能还原氧化铜 |
A.A
B.B
C.C
D.D
| 选项 | 需区别的物质 | 选择的试剂或方法 |
| A | 二氧化锰和氧化铜粉末 | 观察固体颜色 |
| B | 空气、呼出气体 | 伸入燃着的木条 |
| C | 水和酒精 | 取样品闻气味 |
| D | 水和过氧化氢溶液 | 取样品加入少量二氧化锰 |
A.A
B.B
C.C
D.D
| 待鉴别物质 | 鉴别方法1 | 鉴别方法2 | |
| A | 氧气,二氧化碳 | 用燃着的木条 | 通过灼热的铜网 |
| B | 黄铜(铜锌合金),黄金 | 加入硝酸银溶液 | 比较硬度 |
| C | 铝粉,银粉 | 观察颜色 | 加入稀盐酸 |
| D | 氢气,一氧化碳 | 点燃,观察火焰颜色 | 在加热状态下,观察是否能还原氧化铜 |
A.A
B.B
C.C
D.D
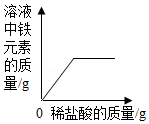
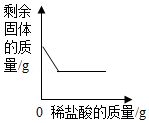
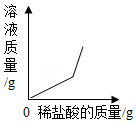
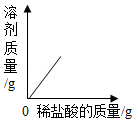
A.b点对应溶液中的溶质是AlCl3
B.该实验是将氧化铝粉末逐渐加入稀盐酸中
C.a点和b点对应溶液蒸发结晶后得到的固体成分不相同
D.a点和b点对应溶液中铝元素的质量相等
A.甲、乙、丙可以分别是单质、氧化物、盐
B.若甲、乙、丙为三种不同的金属,则金属活动性最强的是甲
C.若甲、乙、丙为三种不同的碱,甲常用来改良酸性土壤,乙可以是烧碱,则甲→乙→丙的转化都可体现碱的化学通性
D.若甲、乙、丙为H2SO4、HNO3、HCl中的一种,则乙→丙的转化中一定有白色沉淀生成
| 实验目的 | 测定空气中氧气的含量 | 除去氯化钠固体中的少量碳酸钠 | 区分氯化钠溶液和稀硫酸 | 验证质量守恒定律 |
| 实验方案 |
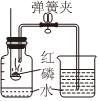
|
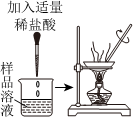 |
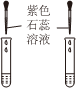
|
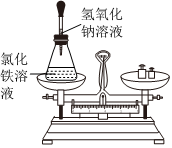 |
| 选项 | A.将红磷改为木炭 | B.将适量稀盐酸改为过量稀盐酸 | C.将石蕊溶液改为酚酞溶液 | D.将氢氧化钠溶液改为硫酸钠溶液 |
A.A
B.B
C.C
D.D
| 选项 | 实验目的 | 实验设计 |
| A | 分离碳酸钙和氯化钙的固体混合物 | 将混合物放入烧杯,加足量水搅拌,充分溶解,过滤 |
| B | 除去二氧化碳中的氯化氢和水蒸气 | 将混合气体依次通过盛有氢氧化钠溶液和浓硫酸的洗气瓶,收集 |
| C | 鉴别氯化铵和硝酸铵两种化肥 | 取样,加水溶解,分别滴加硝酸银溶液,观察现象 |
| D | 除去粗盐中的MgCl2 | 加入适量氢氧化钾溶液,过滤 |
A.A
B.B
C.C
D.D
| 选项 | A | B |
| 实验方案 |
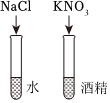
|
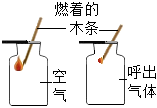 |
| 实验目的 | 探究影响物质溶解性的因素 | 燃着木条证明呼出气体中氧气含量比空气中低 |
| 选项 | C | D |
| 实验方案 | 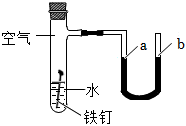 |
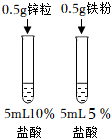 |
| 实验目的 | 证明铁生锈需要氧气和水 | 比较Zn和Fe的金属活动性强弱 |
A.A
B.B
C.C
D.D
| 选项 | 实验目的 | 实验操作 |
| A | 除去ZnCl2溶液中少量FeCl2 | 加入适量锌粉,过滤、洗涤、干燥 |
| B | 除去铜粉中少的量的氧化铜 | 在空气中充分灼烧 |
| C | 鉴别氮气、二氧化碳和氧气 | 将燃着的木条伸入集气瓶中 |
| D | 除去N2中混有的少量O2 | 将气体通过灼热的铜网 |
A.A
B.B
C.C
D.D
A.硫酸溶液、碳酸钾溶液、氯化钡溶液、盐酸
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸溶液
C.碳酸钾溶液、硫酸溶液、盐酸、氯化钡溶液
D.盐酸、硫酸溶液、碳酸钾溶液、氯化钡溶液

mdt@dyw.com
2024-06-12
初中化学 | | 选择题