服务热线
搜题▪组卷
A.甲是碱类物质,丙是单质
B.可用Ba(NO3)2溶液确定乙与氧化铜反应所得溶液的溶质成分
C.丙转化为CuO时固体质量增大
D.CuSO4转化为丙可以选用的物质不止一种
A.甲可能是可溶性碱
B.乙可能是Zn
C.甲与乙一定能发生化学反应
D.图中BaCl2可替换为Ba(NO3)2
A.若甲乙丙是三种常见的酸,则甲一定是硝酸
B.若甲乙丙均含有铜元素,若甲、乙分别为氧化铜、硫酸铜,则丙可以是氢氧化铜或铜
C.若甲乙丙是三种碱,甲可以用来改良酸性土壤,则丙可能为难溶于水的固体
D.若甲乙丙分别是氯化钙、碳酸钙、硝酸钙,则①可以通入二氧化碳实现转化
A.X可能是一种氧化物,能用于灭火
B.反应①中,向CuCl2溶液加入Z,反应后溶液的溶质质量一定减小
C.反应②观察到黑色固体变红,则Y为CuO
D.X、Y、Z中不可能含有同种元素
A.b点对应溶液中的溶质是AlCl3
B.该实验是将氧化铝粉末逐渐加入稀盐酸中
C.a点和b点对应溶液蒸发结晶后得到的固体成分不相同
D.a点和b点对应溶液中铝元素的质量相等
A.向N点对应溶液中加入NaOH溶液,产生蓝色沉淀
B.用Na2CO3溶液可鉴别M和P点溶液中溶质成分
C.N和P点对应溶液中所含离子种类相同
D.该混合物中氧化铜的质量为(a-b)g
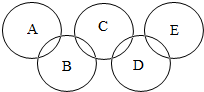 已知A、B、C、D、E分别为稀硫酸、氢氧化钠溶液、二氧化碳、氯化钡溶液、水中的一种,且相连环内的两种物质能发生化学反应,E是常见的溶剂。有关说法不正确的是( )
已知A、B、C、D、E分别为稀硫酸、氢氧化钠溶液、二氧化碳、氯化钡溶液、水中的一种,且相连环内的两种物质能发生化学反应,E是常见的溶剂。有关说法不正确的是( )
A.物质D与物质E反应的化学方程式为H2O+CO2═H2CO3
B.五环中各物质之间相互反应后溶液可能为酸性、中性、碱性
C.将物质A不断加入一定质量的物质B中,溶质质量一直增加
D.五环中各物质之间相互的化学反应涉及了两种基本反应类型
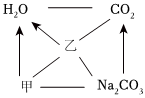 已知甲、乙、Na2CO3三种物质的物质类别不同,“—”表示相连的两种物质能发生化学反应,“→”表示两端的物质通过一步反应可以转化,下列说法不正确的是( )
已知甲、乙、Na2CO3三种物质的物质类别不同,“—”表示相连的两种物质能发生化学反应,“→”表示两端的物质通过一步反应可以转化,下列说法不正确的是( )
A.甲可能是稀盐酸
B.乙一定是碱
C.乙与CO2的反应属于复分解反应
D.甲→H2O可能产生气泡
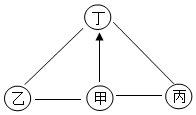 如图所示,甲、乙、丙、丁是初中化学常见的四种物质,甲的稀溶液可用于除铁锈,浓溶液可做气体干燥剂;丁是一种常见的酸,甲与乙反应生成无色气体,丙与丁反应只生成盐和水。图中“—”表示物质间能相互反应,“→”表示物质间能发生一步转化。下列说法正确的是( )
如图所示,甲、乙、丙、丁是初中化学常见的四种物质,甲的稀溶液可用于除铁锈,浓溶液可做气体干燥剂;丁是一种常见的酸,甲与乙反应生成无色气体,丙与丁反应只生成盐和水。图中“—”表示物质间能相互反应,“→”表示物质间能发生一步转化。下列说法正确的是( )
A.甲与丙发生的反应一定是中和反应
B.甲→丁的转化一定会生成可溶性盐
C.物质乙一定是金属
D.乙与丁反应一定有气体生成
| 选项 | 物质 | 主要实验操作 |
| A | 鉴别氧化铜和二氧化锰 | 观察颜色 |
| B | 除去O2中混有的少量水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C | 检验Na2SO4溶液中是否含有H2SO4 | 取样,滴加氯化钡溶液,观察现象 |
| D | 分离KNO3和Ba(NO3)2的混合溶液 | 先加入过量的碳酸钠溶液,搅拌、静置、过滤、洗涤,再分别向滤液、滤渣中加入适量的稀硝酸,搅拌 |
A.A
B.B
C.C
D.D
A.b点对应溶液中的溶质是AlCl3
B.该实验是将氧化铝粉末逐渐加入稀盐酸中
C.a点和b点对应溶液蒸发结晶后得到的固体成分不相同
D.a点和b点对应溶液中铝元素的质量相等
A.该实验是将氧化铜逐渐加入稀盐酸中
B.n点和m点对应溶液中铜元素质量不相等
C.n点和m点对应溶液蒸发结晶后得到的固体成分相同
D.该曲线不能反映溶液中溶剂质量随时间的变化关系
A.甲、乙、丙可以分别是单质、氧化物、盐
B.若甲、乙、丙为三种不同的金属,则金属活动性最强的是甲
C.若甲、乙、丙为三种不同的碱,甲常用来改良酸性土壤,乙可以是烧碱,则甲→乙→丙的转化都可体现碱的化学通性
D.若甲、乙、丙为H2SO4、HNO3、HCl中的一种,则乙→丙的转化中一定有白色沉淀生成

ki@dyw.com
2024-02-07
初中化学 | 九年级上 | 选择题