[解析]
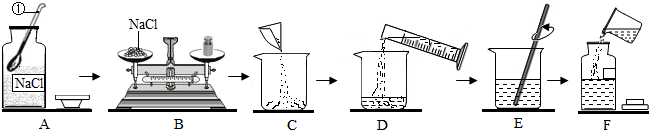
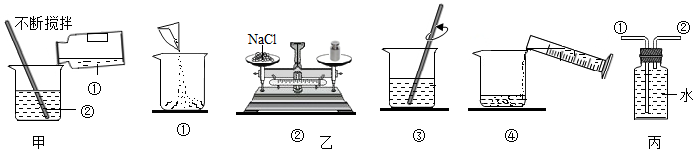
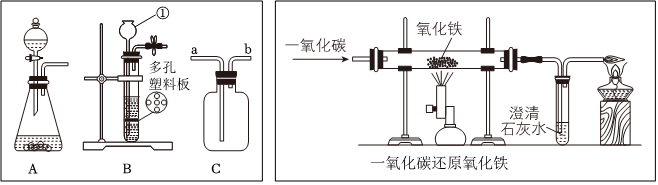
解:(1)图中的玻璃仪器有烧杯、量筒、广口瓶、细口瓶和玻璃棒;
(2)取用固体药品时,为防止污染试剂瓶内的试剂,瓶塞应倒放,图中瓶塞没有倒放,操作错误.
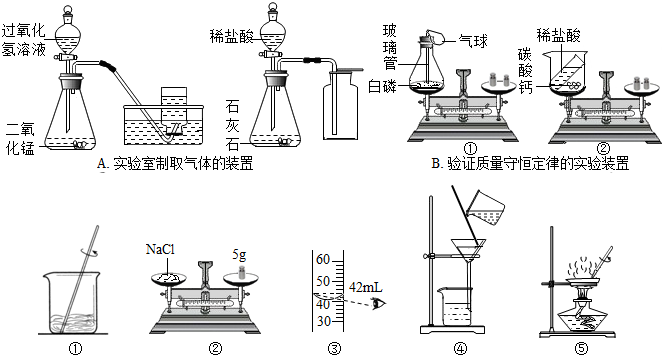
(3)溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为5%的氯化钠溶液,应称量氯化钠的质量是50g×5%=2.5g;
用托盘天平称量2.5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加2g砝码,又将游码移到0.5g处,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl.
(4)溶剂质量=溶液质量﹣溶质质量,则所需水的质量=50g﹣2.5g=47.5g(合47.5mL);选取量筒时,尽量选用能一次量取的最小规格的量筒,应用50mL量筒量取47.5mL水.
(5)E操作的作用是引流;
(6)①B操作中砝码和氯化钠放错托盘,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小,故选项正确.
②D操作中有少量水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项错误.
③D操作中仰视凹液面最低处读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,故选项正确.
④溶液具有均一性,将配制好的溶液转移到试剂瓶时,F操作中溶液洒落有液体溅出,溶质质量分数不变,故选项错误.
故答案为:(1)玻璃棒;(2)瓶塞正放在桌面上;(3)2.5;减少NaCl直到天平平衡;(4)50;(5)引流;(6)①③.