服务热线
搜题▪组卷

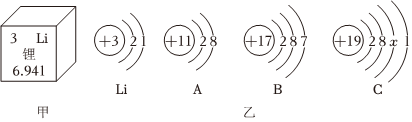
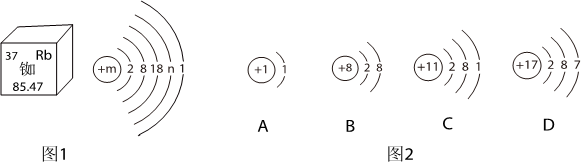
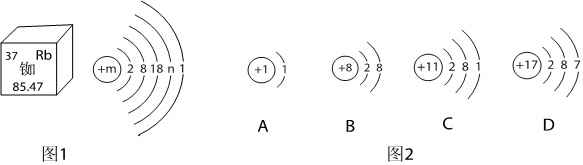
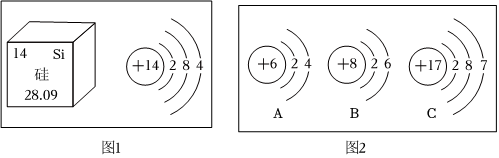
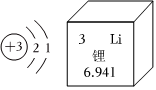
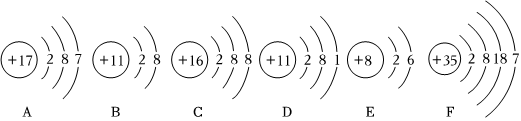
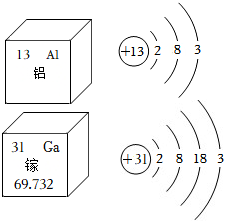 门捷列夫在编制第一张元素周期表时,就预言了类似铝的未知元素(称为“类铝”,即后来发现的镓)的性质。铝和镓在周期表中位置及原子结构示意图如图所示。据图回答下列问题。
门捷列夫在编制第一张元素周期表时,就预言了类似铝的未知元素(称为“类铝”,即后来发现的镓)的性质。铝和镓在周期表中位置及原子结构示意图如图所示。据图回答下列问题。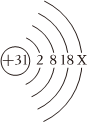 ,其中X= 。
,其中X= 。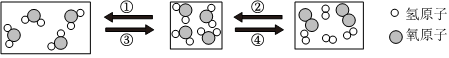 ?
?
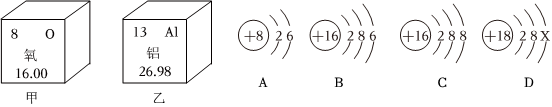
 根据所学知识,回答下列问题。如表为蔗糖的溶解度表:
根据所学知识,回答下列问题。如表为蔗糖的溶解度表:| 温度/℃ | 10 | 20 | 40 | 60 |
| 溶解度/g | 191 | 204 | 238 | 287 |

 2023年,我国汽车产销分别完成3016.1万辆和3009.4万辆,分别同比增长11.6%和12%,产销均首次超过3000万辆,连续15年保持全球第一,其中新能源汽车产销保持高速增长。
2023年,我国汽车产销分别完成3016.1万辆和3009.4万辆,分别同比增长11.6%和12%,产销均首次超过3000万辆,连续15年保持全球第一,其中新能源汽车产销保持高速增长。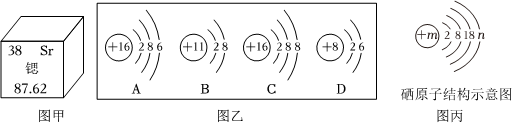

gyy@dyw.com
2021-11-29
初中化学 | 九年级上 | 填空题