服务热线
搜题▪组卷
 |
 |
 |
 |
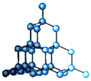
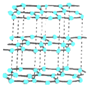
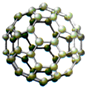
| 甲 | 乙 | 丙 | 丁 |
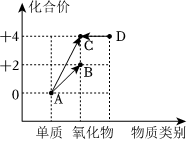 “价—类”二维图反映的是元素化合价与物质类别之间的关系,是我们学习元素及其组成物质相关知识的重要模型和工具。依据碳元素的“价—类”二维图,回答下列问题。
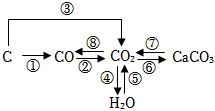
“价—类”二维图反映的是元素化合价与物质类别之间的关系,是我们学习元素及其组成物质相关知识的重要模型和工具。依据碳元素的“价—类”二维图,回答下列问题。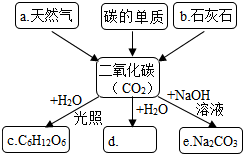 如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略)。请按下列要求填空:
如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略)。请按下列要求填空: 化学兴趣小组的同学们决定走进“碳村庄”,“碳村庄”的部分格局如图所示。
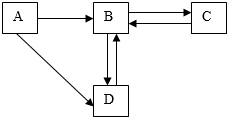
化学兴趣小组的同学们决定走进“碳村庄”,“碳村庄”的部分格局如图所示。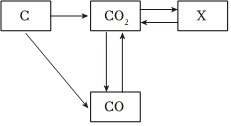 单质碳和部分碳的化合物间转化关系如图所示。
单质碳和部分碳的化合物间转化关系如图所示。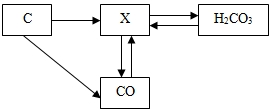 碳和部分碳的化合物间转化关系如图所示。
碳和部分碳的化合物间转化关系如图所示。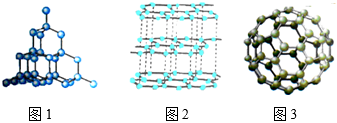
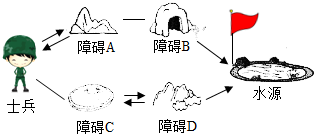 如图化学游戏中,士兵和障碍A~D均表示初中化学常见的物质。最终任务是:士兵要通过两条路径均能顺利越过各种障碍成功找到水源。
如图化学游戏中,士兵和障碍A~D均表示初中化学常见的物质。最终任务是:士兵要通过两条路径均能顺利越过各种障碍成功找到水源。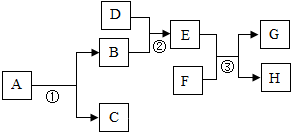
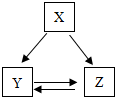 已知X、Y、Z是初中化学常见的三种物质,三种物质均含有同一种元素,它们之间有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)
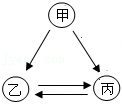
已知X、Y、Z是初中化学常见的三种物质,三种物质均含有同一种元素,它们之间有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)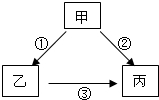 甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如图所示:
甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如图所示: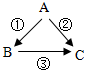 A、B、C为初中化学常见的物质,它们有如下转化关系(部分生成物略去).
A、B、C为初中化学常见的物质,它们有如下转化关系(部分生成物略去).

mdt@dyw.com
2023-12-17
初中化学 | 九年级上 | 填空题