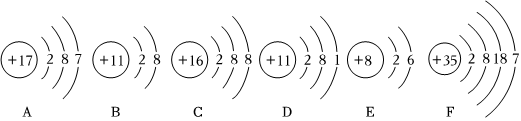
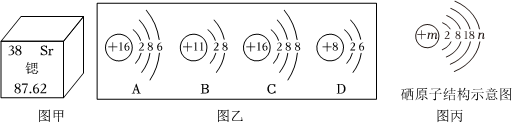
[考点]
电解水实验,元素周期表的特点及其应用,有关元素化合价的计算,根据质量守恒定律判断物质的化学式,
[答案]
(1)+6;
(2)CO;
(3)正;
(4)28.09。
[解析]
解:(1)K2FeO4中,钾元素显+1价,氧元素显﹣2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(﹣2)×4=0,解得x=+6,所以K2FeO4中Fe元素的化合价为+6价;
(2)根据化学方程式可知,反应前的钛原子、氧原子、碳原子、氯原子数目分别为:5、10、6、20,反应后的钛原子、氧原子、碳原子、氯原子数目分别为:5、8、4、20,在化学反应中原子的种类和数目保持不变,2X含有2个氧原子和2个碳原子,X的化学式为CO;
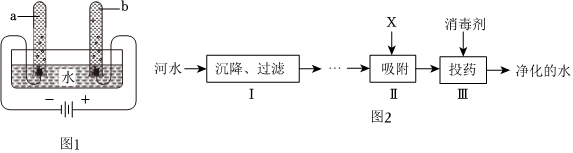
(3)由电解水实验结论“正氧一、负氢二”可知,电解水时氧气在正极产生;
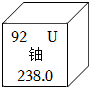
(4)由元素周期表一格中的信息可知,正下方的数字表示相对原子质量,则该元素的相对原子质量为28.09。
故答案为:
(1)+6;
(2)CO;
(3)正;
(4)28.09。
[点评]
本题考查了"电解水实验,元素周期表的特点及其应用,有关元素化合价的计算,根据质量守恒定律判断物质的化学式,",属于"综合题",熟悉题型是解题的关键。
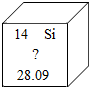 央视栏目《典籍里的中国》展现了中国智慧,其中有许多古今对比。
央视栏目《典籍里的中国》展现了中国智慧,其中有许多古今对比。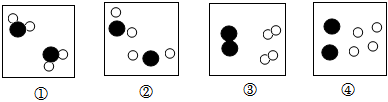

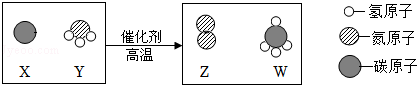 ?
?