服务热线
搜题▪组卷
A.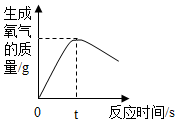
C.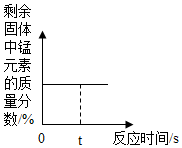
B.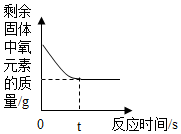
D.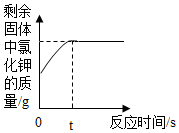
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 0.4 | 2 | 20 | 0.6 |
| 反应后质量(g) | 6 | 2 | X | 5 |
A.x=9
B.乙一定是该反应的催化剂
C.甲可能是化合物或单质
D.该反应可能为电解水
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 70 | 14 | 6 | 10 |
| 反应中质量/g | x | 11 | m | n |
| 反应结束前质量/g | 42 | y | 40 | 10 |
A.x=56
B.y=6
C.m=17
D.n=8
A.参加反应的I2O5的质量等于生成I2的质量
B.参加反应的各物质中的氧原子总数等于生成的CO2 中的氧原子总数
C.反应物所含元素种类与生成物所含元素种类可能不同
D.参加反应的I2O5和CO的质量比等于生成的I2和CO的质量比
A.由二氧化碳和水组成
B.由碳、氢两种元素组成
C.由碳、氢、氧三个元素组成
D.化学式为:C2H5OH
A.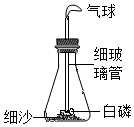
白磷燃烧
C.
蜡烛燃烧
B.
水结冰
D.
镁带在空气中燃烧
A.利用质量守恒定律,可以解释水结冰后质量保持不变
B.某物质燃烧生成二氧化碳和水,根据元素守恒推知该物质中一定含有C、H、O元素
C.水电解生成氢分子和氧分子的个数比为2:1,根据原子守恒推知水分子中氢原子和氧原子个数比为2:1
D.6g氢气和32g氧气反应,根据质量守恒定律推出生成38g水
A.两个实验均可用于测定空气中氧气的含量
B.两个实验均能验证质量守恒定律
C.拉瓦锡的实验中,玻璃钟罩内汞的液面逐渐上升,达到一定高度后不再变化
D.波义耳的实验中,曲颈甑内物质加热后质量增加的现象不能用质量守恒定律来解释
A.Ca(OH)2和H2
C.CaCO3、NaOH和H2
B.NaOH和Ca(OH)2
D.Ca(OH)2、CaCO3和H2
A.若C和D为盐和水,该反应不一定是中和反应
B.若A是氧化铜、C为铜,该反应不一定是置换反应
C.若将20gA和30gB混合,则生成C和D的总质量一定为50g
D.此反应可能是复分解反应
A.反应后图中的X=3
B.该反应为化合反应
C.乙一定是化合物
D.该反应中乙、丁质量变化之比为3:2
A.若X、Y、W、Q均为化合物,则该反应一定属于复分解反应
B.若Y、Q为单质,X、W为化合物,则反应一定属于置换反应
C.若X、Y质量之和为mg,则W、Q质量之和不大于mg
D.若X、Y分别是酸和碱,则W、Q一定有一种物质是盐
| 物质 | X | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 36 |
A.该反应为置换反应
C.X中一定含有碳、氢两种元素
B.表中“待测”值为5
D.反应生成的CO2和H2O的质量比为45:36

zb@dyw.com
2024-06-26
初中化学 | | 选择题