[考点]
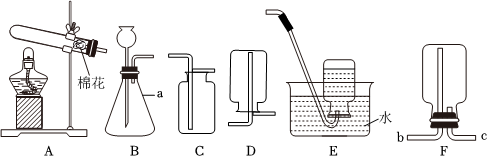
氧气的制取装置,氧气的收集方法,二氧化碳的化学性质,燃烧与燃烧的条件,
[答案]
(1)高锰酸钾;C;
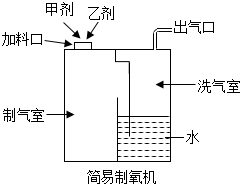
(2)能控制反应速率;
(3)d;碳酸不稳定,遇热易分解;
(4)水中白磷不燃烧。
[解析]
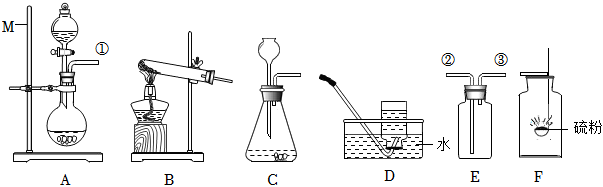
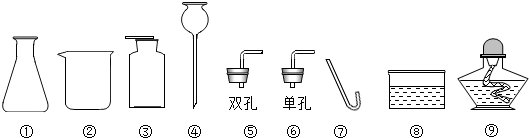
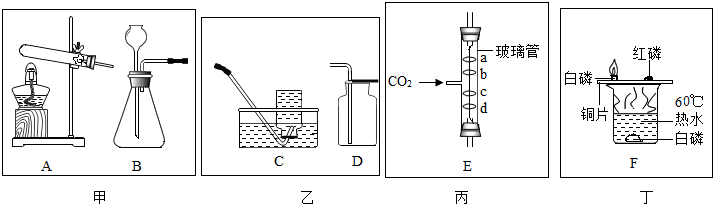
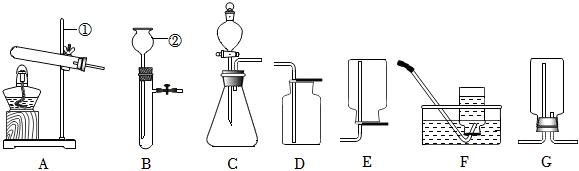
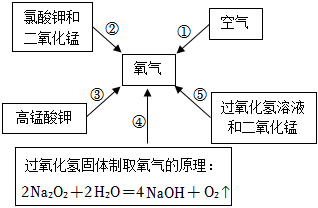
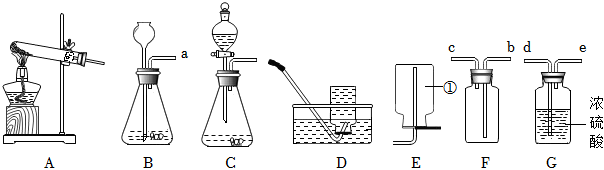
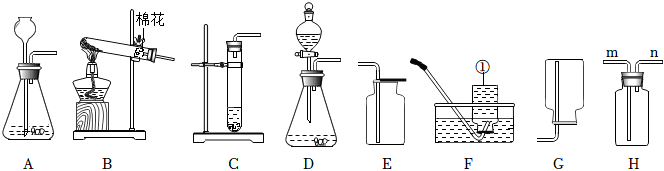
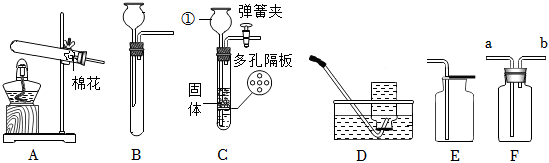
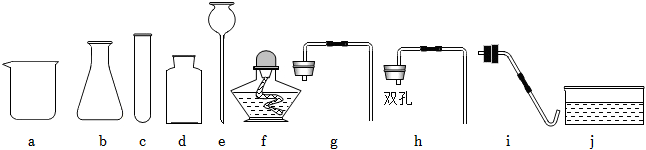
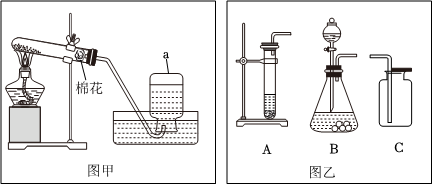
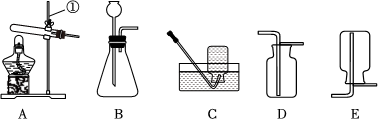
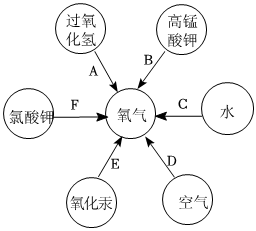
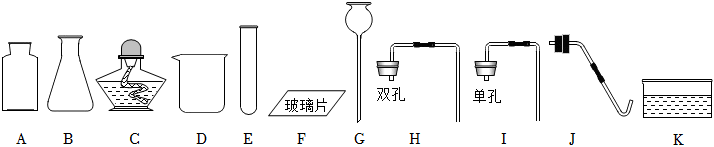
解:(1)甲图中装置属于固体加热型,并且试管口有棉团,制氧气,则选择的药品是高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;氧气不易溶于水,可用排水法来收集较为纯净的氧气;
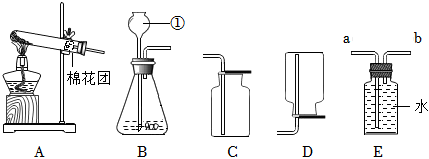
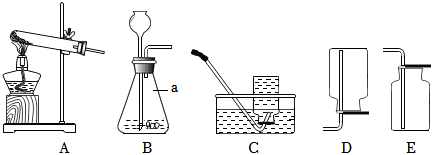
(2)若将B装置中的长颈漏斗换成注射器,则其优点是:能控制反应速率;
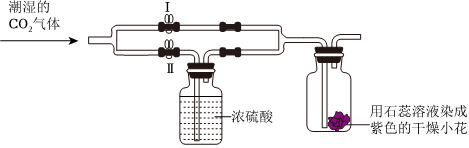
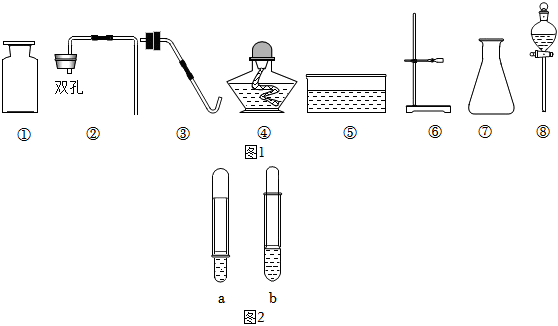
(3)二氧化碳的密度比空气大,且能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色,所以d处的棉球先变红,a处的棉球后变红,而b、c处的棉球不变红;二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红,碳酸不稳定,遇热易分解成二氧化碳和水,当已变红的棉花球用酒精灯微热时,会看到棉球又变成紫色。
(4)在实验中,铜片上的白磷燃烧,铜片上的红磷没有燃烧,热水中的白磷没有燃烧,对比铜片上的白磷燃烧,而铜片上的红磷没有燃烧可知,燃烧需要温度达到可燃物的着火点,对比铜片上的白磷燃烧,而热水中的白磷没有燃烧可知,燃烧需要与氧气充分接触。
故答案为:(1)高锰酸钾;C;
(2)能控制反应速率;
(3)d;碳酸不稳定,遇热易分解;
(4)水中白磷不燃烧。
[点评]
本题考查了"氧气的制取装置,氧气的收集方法,二氧化碳的化学性质,燃烧与燃烧的条件,",属于"综合题",熟悉题型是解题的关键。
 ?
? ?
?