[解析]
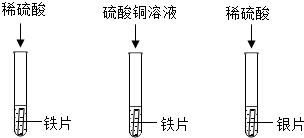
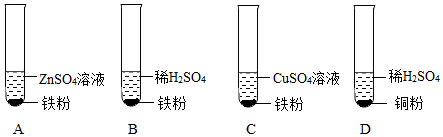
解:(1)试管B内,铁和硫酸铜反应生成硫酸亚铁和铜,观察到铁片表面附着红色固体,溶液由蓝色变为浅绿色。
故填:铁片表面附着红色固体,溶液由蓝色变为浅绿色。
(2)上述三个实验还不能完全证明三种金属的活动性顺序,即不能证明铜和银的活泼性,需要补充一个实验可以是:把铜丝伸入硝酸银溶液中,铜丝表面附着银白色固体,说明铜和硝酸银反应生成硝酸铜和银,即铜比银活泼,反应的化学方程式为:Cu+2AgNO3═2Ag+Cu( NO3)2。
故填:Cu+2AgNO3═2Ag+Cu( NO3)2。
(3)将银、铜、铁中的银、铁分别放入硫酸铜溶液中,可验证三种金属的活动性顺序,这是因为银伸入硫酸铜溶液中时无明显现象,说明铜比银活泼,铁伸入硫酸铜溶液中时,铁表面附着红色固体,说明铁比铜活泼。
故填:硫酸铜。
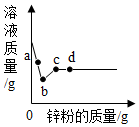
(4)向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉时,锌先和硝酸银反应生成硝酸锌和银,反应过程中溶液质量减小,后和硝酸亚铁反应生成硝酸锌和铁,反应过程中溶液质量增大,b点时锌和硝酸银恰好完全反应,所得溶液中的溶质由反应生成的硝酸锌和没有反应的硝酸亚铁。
故填:ZnNO3)2、Fe( NO3)2。
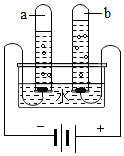 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。
在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题。