服务热线
搜题▪组卷
| 实验方案 | 方案1:向滤液中插入铜丝 | 方案2:向滤液中滴加稀盐酸 |
| 实验现象 | 铜丝表面有银白色固体析出 | |
| 实验结论 | 猜想 成立 | |
| 实验方案 | 方案1:向滤液中插入铜丝 | 方案2:向滤液中滴加稀盐酸 |
| 实验现象 | 铜丝表面有银白色固体析出 | 产生白色沉淀 |
| 实验结论 | 猜想二成立 | |
A.用通入氧气的方法除去CO2中的CO:2CO+O2![]() 2CO2
2CO2
B.用氢氧化钠溶液吸收SO2:2NaOH+SO2═Na2SO4+H2O
C.用一氧化碳还原磁铁矿炼铁:Fe3O4+4CO![]() 3Fe+4CO2
3Fe+4CO2
D.用铁粉和稀盐酸制取少量氢气:2Fe+6HCl═2FeCl3+3H2↑
A.
加热一定量的氯酸钾和二氧化锰的混合物
B.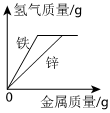
向两份质量相等且溶质质量分数相同的稀硫酸中分别加入铁粉和锌粉
C.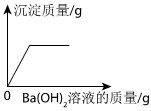
向硫酸钠和盐酸的混合溶液中不断加入Ba(OH)2溶液
D.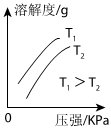
CO2的溶解性随温度和压强的变化
A.工业上用高温煅烧石灰石的方法制备生石灰:CaCO3![]() CaO+CO2
CaO+CO2
B.医疗上用氢氧化镁中和过多的胃酸:Mg(OH)2+HCl═MgCl2+H2O
C.正常雨水的pH小于7的原因:CO2+H2O═H2CO3
D.改良酸性土壤:2NaOH+H2SO4═Na2SO4+2H2O
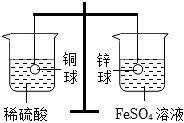 某学习小组同学利用杠杆原理设计如图所示实验,实验前在杠杆的两端分别挂质量相等的铜球和锌球(均已打磨),此时杠杆平衡,然后将两个金属球分别浸没在盛有稀硫酸和FeSO4溶液的烧杯中进行实验。下列有关说法正确的是( )
某学习小组同学利用杠杆原理设计如图所示实验,实验前在杠杆的两端分别挂质量相等的铜球和锌球(均已打磨),此时杠杆平衡,然后将两个金属球分别浸没在盛有稀硫酸和FeSO4溶液的烧杯中进行实验。下列有关说法正确的是( )
A.实验中观察到左端烧杯中溶液变为蓝色
B.右端烧杯中反应后的溶液里一定有ZnSO4
C.该实验可得出三种金属的活动性顺序为Zn>Fe>Cu
D.实验结束后移走烧杯,杠杆仍保持平衡
A.CaO→Ca(OH)2
C.CaCO3→CaO
B.CaO→CaCO3
D.Ca(OH)2→CaCO3
A.若滤液为无色溶液,则可以证明金属的活动性Mg>Cu>Ag
B.若向滤渣中加入稀盐酸,没有气泡产生,则滤液中一定含有Mg(NO3)2、Cu(NO3)2
C.若滤液为蓝色溶液,则滤液中至少含有三种金属离子
D.若加入镁的质量为2.4g,则滤渣的质量一定大于2.4g
A.t1时,产生气体的质量:X>Y
B.t2时,消耗金属的质量:X>Y
C.t3时,消耗金属的质量:X=Y
D.t3时,消耗盐酸的质量:X=Y
A.滤液中一定不含有硝酸银
C.滤液中一定含有硝酸银和硝酸锌
B.滤渣中只含银
D.滤渣中一定含有锌、铁和银
A.
表示加热等质量的氯酸钾制取氧气
C.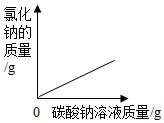
表示向混有盐酸的氯化钙溶液中逐滴加入碳酸钠溶液
B.
表示向一定质量的稀盐酸中加入过量的CuO粉末
D.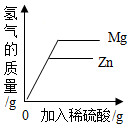
表示向等质量的镁、锌中分别加入稀硫酸
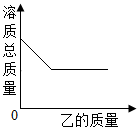
| 选项 | 甲 | 乙 |
| A | 硫酸铜溶液 | 镁 |
| B | 氢氧化钡溶液 | 稀硫酸 |
| C | 氯化钙溶液 | 二氧化碳 |
| D | 不饱和的硝酸钾溶液 | 硝酸钾固体 |
 |
 |
 |
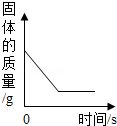 |
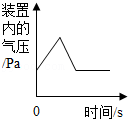
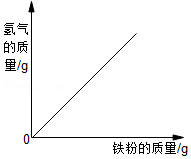
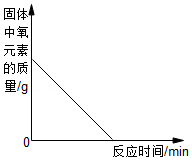
| A.足量镁条在密闭容器中燃烧 | B.向一定质量的稀硫酸中加入足量的铁粉 | C.一定条件下氧化铜和炭粉恰好完全反应 | D.将铁钉加入足量的硫酸铜溶液中 |
A.步骤①和②的顺序不能颠倒
B.加入过量氢氧化钠溶液的目的是除尽Mg2+
C.步骤③中所得沉淀的成分是碳酸镁和碳酸钙
D.步骤④中只发生了中和反应
A.
电离水生成氢气和氧气,说明水中含有2个氢原子和1个氧原子
B.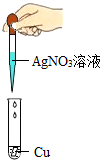
铜片表面出现银白色物质,溶液由无色变成蓝色,说明铜比银活泼
C.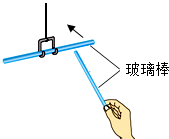
用丝绸摩擦过的两根玻璃棒靠近后,一根远离,说明同种电荷互相排斥
D.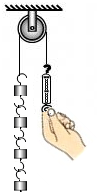
测力计示数与钩码重相等,说明使用定滑轮不能省力但可以改变力的方向

dyhx2022
2017-07-21
初中化学 | | 选择题