服务热线
搜题▪组卷
 ?
? ?
?
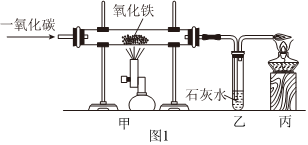
 某化学兴趣小组同学利用图中一氧化碳与氧化铁反应所示装置模拟炼铁:
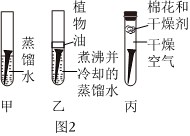
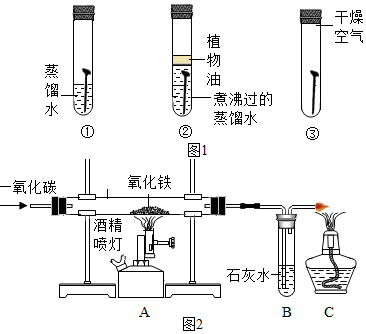
某化学兴趣小组同学利用图中一氧化碳与氧化铁反应所示装置模拟炼铁: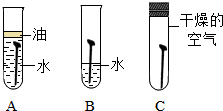 全世界每年因生锈损失的钢铁,约占世界年产量的四分之一.某学生想探究铁生锈的条件,他将干净的铁钉放入A、B、C三支试管中,分别进行如图所示实验.
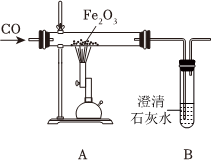
全世界每年因生锈损失的钢铁,约占世界年产量的四分之一.某学生想探究铁生锈的条件,他将干净的铁钉放入A、B、C三支试管中,分别进行如图所示实验.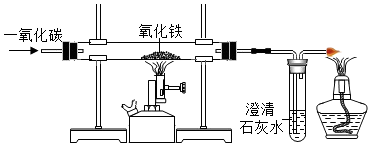 早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
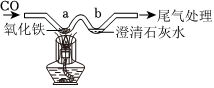
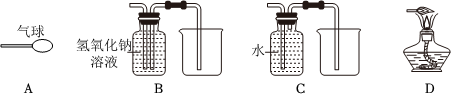
 化学与生活关系密切,请结合所学知识回答下列问题:
化学与生活关系密切,请结合所学知识回答下列问题: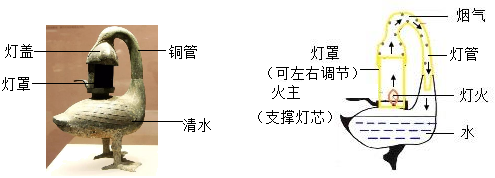

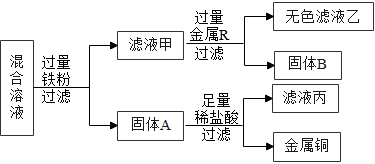
 高铁已成为中国的名片。结合如图所示信息回答下列问题。
高铁已成为中国的名片。结合如图所示信息回答下列问题。
wpo@dyw.com
2023-12-15
初中化学 | 九年级上 | 填空题