服务热线
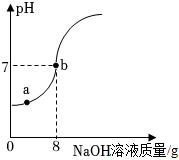 欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取20g稀硫酸样品于烧杯中,将20%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所。请回答下列问题:
欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取20g稀硫酸样品于烧杯中,将20%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所。请回答下列问题: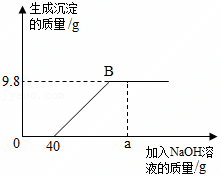
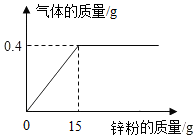
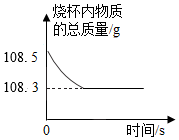 实验小组称取10g生铁样品于烧杯中,然后向其中加入100g稀硫酸,恰好完全反应(杂质不与酸反应),称得反应前后烧杯内物质的总质量随时间的变化关系如图所示。请完成下列分析与计算:
实验小组称取10g生铁样品于烧杯中,然后向其中加入100g稀硫酸,恰好完全反应(杂质不与酸反应),称得反应前后烧杯内物质的总质量随时间的变化关系如图所示。请完成下列分析与计算: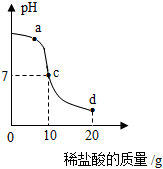 将20g稀盐酸逐渐加入到20g溶质质量分数为4%的氢氧化钠溶液中,如图为所加稀盐酸与溶液pH的变化情况。分析并计算:
将20g稀盐酸逐渐加入到20g溶质质量分数为4%的氢氧化钠溶液中,如图为所加稀盐酸与溶液pH的变化情况。分析并计算:| 反应前 | 反应后 | ||
| 实验 数据 |
烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 152.0g | 12.0g | 159.6g | |
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 8 | 4 | 2 | 2 |
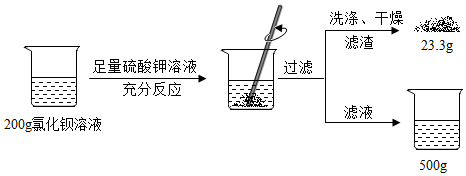
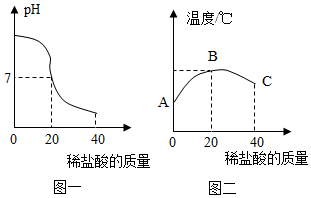 将40g稀盐酸逐滴加入到20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴加,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中热量损失)。试回答:
将40g稀盐酸逐滴加入到20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴加,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中热量损失)。试回答:| 氢氧化钾溶液的质量/g | 5.6 | 11.2 | 22.4 | 33.6 |
| 生成沉淀的质量/g | 0.145 | 0.29 | 0.58 | 0.58 |

dyczhxyn
2024-04-05
初中化学 | | 计算题